Что генная инженерия в биологии. Что такое генная инженерия и что она изучает? Объекты генной инженерии
Введение
В своей работе я раскрываю тему генной инженерии. Возможности, открываемые генетической инженерией перед человечеством, как в области фундаментальной науки, так и во многих других областях, весьма велики и нередко даже революционны.
Так, она позволяет осуществлять индустриальное массовое производство нужных белков, значительно облегчает технологические процессы для получения продуктов ферментации - энзимов и аминокислот, в будущем может применяться для улучшения растений и животных, а также для лечения наследственных болезней человека.
Таким образом, генная инженерия, будучи одними из магистральных направлений научно-технического прогресса, активно способствует ускорению решения многих задач, таких, как продовольственная, сельскохозяйственная, энергетическая, экологическая.
Но особенно большие возможности генная инженерия открывает перед медициной и фармацевтикой, поскольку применение генной инженерии может привести к коренным преобразованиям медицины.
1. Сущность генетической инженерии.
1.1. История генной инженерии.
Генная инженерия появилась благодаря работам многих исследователей в разных отраслях биохимии и молекулярной генетики.
На протяжении многих лет главным классом макромолекул считали белки. Существовало даже предположение, что гены имеют белковую природу.
Лишь в 1944 году Эйвери, Мак Леод и Мак Карти показали, что носителем наследственной информации является ДНК.
С этого времени начинается интенсивное изучение нуклеиновых кислот. Спустя десятилетие, в 1953 году Дж. Уотсон и Ф. Крик создали двуспиральную модель ДНК. Именно этот год принято считать годом рождения молекулярной биологии.
На рубеже 50-60-х годов были выяснены свойства генетического кода, а к концу 60-х годов его универсальность была подтверждена экспериментально.
Шло интенсивное развитие молекулярной генетики, объектами которой стали кишечная палочка (E. Coli), ее вирусы и плазмиды.
Были разработаны методы выделения высокоочищенных препаратов неповрежденных молекул ДНК, плазмид и вирусов.
ДНК вирусов и плазмид вводили в клетки в биологически активной форме, обеспечивая ее репликацию и экспрессию соответствующих генов.
В 70-х годах был открыт ряд ферментов, катализирующих реакции превращения ДНК. Особая роль в развитии методов генной инженерии принадлежит рестриктазам и ДНК-лигазам.
Историю развития генетической инженерии можно условно разделить на три этапа:
Первый этап связан с доказательством принципиальной возможности получения рекомбинантных молекул ДНК in vitro. Эти работы касаются получения гибридов между различными плазмидами. Была доказана возможность создания рекомбинантных молекул с использованием исходных молекул ДНК из различных видов и штаммов бактерий, их жизнеспособность, стабильность и функционирование.
Второй этап связан с началом работ по получению рекомбинантных молекул ДНК между хромосомными генами прокариот и различными плазмидами, доказательством их стабильности и жизнеспособности.
Третий этап - начало работ по включению в векторные молекулы ДНК (ДНК, используемые для переноса генов и способные встраиваться в генетический аппарат клетки-реципиента) генов эукариот, главным образом, животных.
Формально датой рождения генетической инженерии следует считать 1972 год, когда в Стенфордском университете П. Берг и С. Коэн с сотрудниками создали первую рекомбинантную ДНК, содержавшую фрагменты ДНК вируса SV40, бактериофага и E. coli.
1.2. Понятие о генной инженерии
Одним из разделов молекулярной генетики и молекулярной биологии, который нашел наибольшее практическое приложение, является генная инженерия.
Генная инженерия – это сумма методов, позволяющих переносить гены из одного организма в другой, или – это технология направленного конструирования новых биологических объектов.
Родившись в начале 70-х годов, она добилась сегодня больших успехов. Методы генной инженерии преобразуют клетки бактерий, дрожжей и млекопитающих в «фабрики» для масштабного производства любого белка.
Это дает возможность детально анализировать структуру и функции белков и использовать их в качестве лекарственных средств.
В настоящее время кишечная палочка (E. coli) стала поставщиком таких важных гормонов как инсулин и соматотропин.
Ранее инсулин получали из клеток поджелудочной железы животных, поэтому стоимость его была очень высока. Для получения 100г кристаллического инсулина требуется 800-1000кг поджелудочной железы, а одна железа коровы весит 200-250грамм. Это делало инсулин дорогим и труднодоступным для широкого круга диабетиков.
Инсулин состоит из двух полипептидных цепей А и В длиной 20 и 30 аминокислот. При соединении их дисульфидными связями образуется нативный двухцепочечный инсулин.
Было показано, что он не содержит белков E. coli, эндотоксинов и других примесей, не дает побочных эффектов, как инсулин животных, а по биологической активности от него не отличается.
Соматотропин - гормон роста человека, секретируемый гипофизом. Недостаток этого гормона приводит к гипофизарной карликовости. Если вводить соматотропин в дозах 10 мг на 1 кг веса три раза в неделю, то за год ребенок, страдающий от его недостатка, может подрасти на 6 см.
Ранее его получали из трупного материала, из одного трупа: 4 - 6 мг соматотропина в пересчете на конечный фармацевтический препарат. Таким образом, доступные количества гормона были ограничены, кроме того, гормон, получаемый этим способом, был неоднороден и мог содержать медленно развивающиеся вирусы.
Компания «Genentec» в 1980 году разработала технологию производства соматотропина с помощью бактерий, который был лишен перечисленных недостатков. В 1982 году гормон роста человека был получен в культуре E. coli и животных клеток в институте Пастера во Франции, а с 1984 года начато промышленное производство инсулина и в СССР.
1.3. Цели и задачи генной инженерии
Цель прикладной генетической инженерии заключается в конструировании таких рекомбинантных молекул ДНК, которые при внедрении в генетический аппарат придавали бы организму свойства, полезные для человека.
На технологии рекомбинантных ДНК основано получение высокоспецифичных ДНК-зондов, с помощью которых изучают экспрессию генов в тканях, локализацию генов в хромосомах, выявляют гены, обладающие родственными функциями (например, у человека и курицы). ДНК-зонды также используются в диагностике различных заболеваний.
Технология рекомбинантных ДНК сделала возможным нетрадиционный подход «белок-ген», получивший название «обратная генетика». При таком подходе из клетки выделяют белок, клонируют ген этого белка, модифицируют его, создавая мутантный ген, кодирующий измененную форму белка. Полученный ген вводят в клетку. Таким способом можно исправлять дефектные гены и лечить наследственные заболевания.
Если гибридную ДНК ввести в оплодотворенное яйцеклетку, могут быть получены трансгенные организмы, передающие мутантный ген потомками.
Генетическая трансформация животных позволяет установить роль отдельных генов и их белковых продуктов как в регуляции активности других генов, так и при различных патологических процессах.
Технология рекомбинантных ДНК использует следующие методы:
·специфическое расщепление ДНК рестрицирующими нуклеазами, ускоряющее выделение и манипуляции с отдельными генами;
·быстрое секвенирование всех нуклеотидов очищенном фрагменте ДНК, что позволяет определить границы гена и аминокислотную последовательность, кодируемую им;
·конструирование рекомбинантной ДНК;
·гибридизация нуклеиновых кислот, позволяющая выявлять специфические последовательности РНК или ДНК с большей точностью и чувствительностью;
·клонирование ДНК: амплификация in vitro с помощью цепной полимеразной реакции или введение фрагмента ДНК в бактериальную клетку, которая после такой трансформации воспроизводит этот фрагмент в миллионах копий;
·введение рекомбинантной ДНК в клетки или организмы.
2.
2.1. Выделение генов, содержащих необходимую информацию.
Получение генов возможно несколькими путями: выделением из ДНК, химико-ферментным синтезом и ферментным синтезом.
Выделение генов из ДНК проводят с помощью рестриктаз, катализирующих расщепление ДНК на участках, имеющих определенные нуклеотидные последовательности (4–7 нуклеотидных пар). Расщепление можно проводить по середине узнаваемого участка нуклеотидных пар; при этом обе нити ДНК «разрезаются» на одном уровне. Образующиеся фрагменты ДНК имеют так называемые «тупые» концы. Возможно расщепление ДНК со сдвигом, при этом одна из нитей выступает на несколько нуклеотидов. Образуемые при этом «липкие» концы в силу своей комплементарности вступают во взаимодействие. Нуклеотидную последовательность с липкими концами можно присоединить к вектору (предварительно обработанному той же рестриктазой), Превратить в кольцевую в результате сшивания лигазами взаимно комплиментарных концов. Метод имеет существенные недостатки, так как достаточно трудно подобрать действие ферментов для строгого вычленения нужного гена. Вместе с геном захватываются «лишние» нуклеотиды или, наоборот, ферменты отрезают часть гена, превращая его в функционально неполноценный.
Химико-ферментный синтез применяют в том случае, если известна первичная структура белка или пептида, синтез которого кодирует ген. Необходимо полное знание нуклеотидной последовательности гена. Этот метод позволяет точно воссоздать нужную последовательность нуклеотидов, а также вводить в гены участки узнавания рестриктаз, регуляторных последовательностей и пр. Метод состоит из химического синтеза одно цепочечных фрагментов ДНК (олигонуклеотидов) за счет поэтапного образования эфирных связей между нуклеотидами, обычно 8–16-звенных. В настоящее время существуют «генные машины», которые под контролем микропроцессора очень быстро синтезируют специфические короткие последовательности одноцепочечной ДНК
Нужная последовательность оснований вводится на клавишный пульт управления. Микропроцессор открывает клапаны, через которые с помощью насоса в синтезирующую колонку последовательно поступают нукеотиды, а также необходимые реагенты и растворители. Колонка наполена бусинками кремния, на которых собираются молекулы ДНК. В данном устройстве возможен синтез цепей длиной до 40 нуклеотидов со скростью 1 нуклеотид за 30 минут. Полученные олигонуклеотиды с помощью ДНК-лигазы сшиваются между собой с образованием двуцепочечного нуклеотида. С помощью данного метода были получены гены А- и В-цепей инсулина, проинсулина, соматостатина и др.
Ферментный синтез гена на основе выделенной матричной РНК(мРНК) является в настоящее время наиболее распространенным методом. Сначала из клеток выделяют матричные РНК, среди которых присуттвует мРНК, кодируемая геном, который требуется выделить. Затем в одобранных условиях на выделенной из клетки мРНК, как на матрице, с помощью обратной транскриптазы (ревертазы) синтезируется нить ДНК, комплиментарная мРНК (кДНК). Полученная комплиментарная ДНК (кДНК) служит матрицей для синтеза второй нити ДНК с использованием ДНК-полимеразы или ревертазы. Затравкой при этом служит олигонуклеотид, комплиментарный 3’-концу мРНК; новая цепь ДНК образуется из дезоксинуклеозидтрифосфатов в присутствии ионов магния.
Метод с большим успехом применен для получения в 1979 г. гена гормона роста человека (соматотропина). Полученный тем или иным способом ген содержит информацию о структуре белка, но сам не может ее реализовать. Поэтому нужны дополнительные механизмы для управления действием гена. Перенос генетической информации в клетку реципиента осуществляется в составе вектора. Вектор – это, как правило, кольцевая молекула ДНК, способная к самостоятельной репликации. Ген вместе с вектором образует рекомбинантную ДНК.
2.2. Подбор векторов (вирусы, плазмиды), способных к самостоятельной репликации в клетке реципиента.
Под понятием «вектор» понимается молекула нуклеиновой кислоты, способная после введения в клетку к автономному существованию за счет наличия в ней сигналов репликации и транскрипции.
Векторные молекулы должны обладать следующими свойствами:
1) способностью автономно реплицироваться в клстке-реципиенте, то есть быть самостоятельным репликоном;
В зависимости от целей эксперимента векторы можно условно разделить на две группы: 1) используемые для клонирования и амплификации нужного гена; 2) специализированные, применяемые для экспрессии встроенных чужеродных генов. Вторая группа векторов объединяет векторы, призванные обеспечить синтез белковых продуктов клонированных генов. Векторы для экспрессии содержат последовательности ДНК, которые необходимы для транскрипции клонированных копий генов и трансляции их мРНК в штаммах клеток.
В качестве прокариотических векторов используются плазмиды, бактериофаги; в качестве эукариотических векторов применяют вирусы животных и растений, векторы на основе 2 мкм дрожжей и митохондрий и ряд искусственно сконструированных векторов, способных реплицироваться как в бактериальных, так и в эукариотических клетках (челночные векторы).
Плазмиды - это внехромосомные генетические элементы про- и эукариот, которые автономно реплицируются в клетках. Большинство плазмидных векторов получено на основе природных плазмид ColE1, pMB1 и p15A.
Бактериальные плазмиды делят на два класса. Одни плазмиды (например, хорошо изученный фактор F, определяющий пол у E.coli) сами способны переходить из клетки в клетку, другие такой способностью не обладают. По ряду причин, и прежде всего для предотвращения неконтролируемого распространения потенциально опасного генетического материала, подавляющее большинство бактериальных плазмидных векторов создано на базе плазмид второго класса. Многие природные плазмиды уже содержат гены, определяющие устойчивость клеток к антибиотикам (продукты этих генов - ферменты, модифицирующие или расщепляющие антибиотические вещества). Кроме того, в эти плазмиды при конструировании векторов вводятся дополнительные гены, определяющие устойчивость к другим антибиотикам.
На рис. 1 показан один из самых распространенных плазмидных векторов E.coli - pBR322. Он сконструирован на базе детально изученной плазмиды E.coli - колициногенного фактора ColE1 - и содержит ориджин репликации этой плазмиды. Особенность плазмиды ColE1 (и pBR322 соответственно) состоит в том, что в присутствии ингибитора синтеза белка антибиотика хлорамфеникола (опосредованно ингибирующего репликацию хозяйской хромосомы) ее число в E.coli возрастает от 20-50 до 1000 молекул на клетку, что позволяет получать большие количества клонируемого гена. При конструировании вектора pBR322 из исходных плазмид был делегирован целый ряд «лишних» сайтов для рестриктаз.
В настоящее время наряду с множеством удобных векторных систем для E.coli сконструированы плазмидные векторы для ряда других грамотрицательных бактерий (в том числе таких промышленно важных, как Pseudomonas, Rhizobium и Azotobacter), грамположительных бактерий (Bacillus), низших грибов (дрожжи) и растений.
Плазмидные векторы удобны для клонирования относительно небольших фрагментов (до 10 тыс. пар оснований) геномов небольших размеров. Если же требуется получить клонотеку (или библиотеку) генов высших растений и животных, общая длина генома которых достигает огромных размеров, то обычные плазмидные векторы для этих целей непригодны. Проблему создания библиотек генов для высших эукариот удалось решить с использованием в качестве клонирующих векторов производных бактериофага l.
Среди фаговых векторов наиболее удобные системы были созданы на базе геномов бактериофагов l и М13 E.coli. ДНК этих фагов содержит протяженные области, которые можно делегировать или заменить на чужеродную ДНК, не затрагивая их способности реплицироваться в клетках E.coli. При конструировании семейства векторов на базе ДНК l фага из нее сначала (путем делений коротких участков ДНК) были удалены многие сайты рестрикции из области, не существенной для репликации ДНК, и оставлены такие сайты в области, предназначенной для встраивания чужеродной ДНК. В эту же область часто встраивают маркерные гены, позволяющие отличить рекомбинантную ДНК от исходного вектора. Такие векторы широко используются для получения «библиотек генов». Размеры замещаемого фрагмента фаговой ДНК и соответственно встраиваемого участка чужеродной ДНК ограничены 15-17 тыс. нуклеотидных остатков, так как рекомбинантный фаго - вый геном, который на 10% больше или на 75% меньше генома дикого l фага, уже не может быть упакован в фаговые частицы.
Рисунок 1. Детальная рестрикционная карта плазмиды pBR322.
Таких ограничений теоретически не существует для векторов, сконструированных на базе нитчатого бактериофага М13. Описаны случаи, когда в геном этого фага была встроена чужеродная ДНК длиной около 40 тыс. нуклеотидных остатков. Известно, однако, что фаг М13 становится нестабильным, когда длина чужеродной ДНК превышает 5 тыс. нуклеотидных остатков. Фактически же векторы, полученные из ДНК фага М13, используются главным образом для секвенирования и мутагенеза генов, и размеры встраиваемых в них фрагментов намного меньше.
Эти векторы конструируются из реплекативной (двутяжевой) формы ДНК фага М13, в которую встроены «полилинкерные» участки (пример такой конструкции показан на рис. 5). В фаговую частицу ДНК включается в виде однотяжевой молекулы. Таким образом, этот вектор позволяет получать клонированный ген или его фрагмент как в двутяжевой, так и в однотяжевой форме. Однотяжевые формы рекомбинантных ДНК широко используются в настоящее время при определении нуклеотидной последовательности ДНК методом Сэнгера и для олигодезоксинуклеотид-направленного мутагенеза генов.
Перенос чужеродных генов в клетки животных осуществляется с помощью векторов, полученных из ДНК ряда хорошо изученных вирусов животных - SV40, некоторых аденовирусов, вируса папиломы быка, вируса оспы и так далее. Конструирование этих векторов проводится по стандартной схеме: удаление «лишних» сайтов для рестриктаз, введение маркерных генов в области ДНК, не существенные для ее репликации (например, гена тимидин-киназы (tk) из HSV (вируса герпеса)), введение регуляторных районов, повышающих уровень экспрессии генов.
Удобными оказались так называемые «челночные векторы», способные реплицироваться как в клетках животных, так и в клетках бактерий. Их получают, сшивая друг с другом большие сегменты векторов животных и бактерий (например, SV40 и pBR322) так, чтобы районы, ответственные за репликацию ДНК, остались незатронутыми. Это позволяет проводить основные операции по конструированию вектора в бактериальной клетке (что технически намного проще), а затем полученную рекомбинантную ДНК использовать для клонирования генов в животной клетке.
Рисунок 2. Рестрикционная карта вектора М13 mp8.
2.3. Получение рекомбинантной ДНК.
Суть конструирования рекомбинантных ДНК заключается во встраивании фрагментов ДНК, среди которых находится интересующий нас участок ДНК, в так называемые векторные молекулы ДНК (или просто векторы) - плазмидные или вирусные ДНК, которые могут быть перенесены в клетки про- или эукариот и там автономно репли-цироваться. На следующем этапе проводится отбор тех клеток, которые несут в себе рекомбинантные ДНК (с помощью маркерных признаков, которыми обладает сам вектор), и затем индивидуальных клонов с интересующим нас сегментом ДНК (используя признаки или пробы, специфичные для данного гена или участка ДНК).
При решении ряда научных и биотехнологических задач конструирование рекомбинантных ДНК требует также создания систем, в которых обеспечивается максимальная экспрессия клонируемого гена.
Существует три основных способа встраивания чужеродной ДНК в векторные молекулы. В первом случае 3"-концы фрагментов ДНК, среди которых находится интересующий нас участок ДНК (ген или его сегмент, регуляторный район), с помощью фермента терминальной нуклеотидилтрансферазы наращиваются гомополинуклеотидной последовательностью (например, поли (Т)). 3"-концы линейной формы векторной ДНК тем же способом наращиваются комплементарной ей гомополинуклеотидной последовательностью (то есть поли (А)). Это позволяет соединить две молекулы ДНК путем комплементарного спаривания искусственно полученных «липких» концов.
Во втором случае «липкие» концы создаются с помощью расщепления молекул ДНК (как векторной, так и содержащей интересующий нас фрагмент) одной из эндонуклеаз рестрикции (рестриктаз). Рестриктазы характеризуются исключительно высокой специфичностью. Они «узнают» в ДНК последовательность из нескольких нуклеотидных остатков и расщепляют в них строго определенные межнуклеотидные связи. Поэтому даже в ДНК больших размеров рестриктазы вносят ограниченное число разрывов.
Третий способ представляет собой комбинацию двух первых, когда липкие концы ДНК, образованные рестриктазой, удлиняются синтетическими последовательностями (рис. 3).
Концы фрагментов ДНК можно превратить в «липкие», наращивая их двутяжевыми олигонуклеотидами («линкерами»), в состав которых входит участок узнавания рестрикта-
Рисунок 3. Схема конструирования рекомбинантной ДНК с помощью рестриктаз PstI и поли(G)- поли(С)-линкера.
зой. Обработка такого фрагмента данной рестриктазой делает его пригодным для встраивания в векторную молекулу ДНК, расщепленную той же рестриктаэой. Часто в качестве «линкера» применяются полинуклеотидные фрагменты, которые содержат специфические участки сразу для нескольких рестриктаз (их называют «полилинкерами»).
После встраивания чужеродной ДНК в вектор их ковалентное сшивание осуществляется ДНК-лигазой. Если же размер бреши в рекомбинированной молекуле превышает одну фосфодиэфирную связь, она застраивается in vitro с помощью ДНК-полимеразы или in vivo с помощью репарирующих систем клетки.
2.4. Введение рекомбинантной ДНК в клетку – реципиент
Перенос рекомбинантных ДНК осуществляется путем трансформации или конъюгации. Трансформация – это процесс изменения генетических свойств клетки в результате проникновения в нее чужеродной ДНК. Впервые она была обнаружена у пневмококков Ф. Гиффитом, который показал, что некоторые клетки невирулентных штаммов бактерий при заражении ими мышей совместно с вирулентными штаммами приобретают патогенные свойства. В дальнейшем трансформация была продемонстрирована и изучена у различных видов бактерий. Установлено, что к трансформации способны лишь некоторые, так называемые «компетентные», клетки (способные включать чужеродную ДНК и синтезирующие особый трансформирующий белок). Компетентность клетки определяется также факторами внешней среды. Этому может способствовать обработка клеток полиэтиленгликолем или хлоридом кальция. После проникновения в клетку одна из нитей рекомбиантной ДНК деградирует, а другая за счет рекомбинации с гомологичным участком реципиентной ДНК может включиться в хромосому или внехромосомную единицу. Трансформация является наиболее универсальным способом передачи генетической информации и имеет наибольшее значение для генетических технологий.
Конъюгация – один из способов обмена генетического материала, при котором происходит однонаправленный перенос генетической информации от донора к реципиенту. Этот перенос находится под контролем особых конъюгативных плазмид (фактор фертильности). Перенос информации от донорской клетки в реципиентную осуществляется через специальные половые ворсинки (пили). Возможна передача информации и с помощью неконъюгативных плазмид при участии плазмид-помощниц.Передача всего набора генов вируса или фага, приводящая к развитию в клетке фаговых частиц, называется трансфекцией. Методика применительно к бактериальным клеткам включает получение сферопластов, очистку инкубационной среды от нуклеаз и добавление очищенной фаговой ДНК (присутствие протаминсульфата повышает эффективность трансфекции). Методика применима к животным и растительным клеткам с участием специальных челночных вирусных векторов.
3.
В применении к человеку генная инженерия могла бы применяться для лечения наследственных болезней. Однако, технически, есть существенная разница между лечением самого пациента и изменением генома его потомков.
Задача изменения генома взрослого человека несколько сложнее, чем выведение новых генно-инженерных пород животных, поскольку в данном случае требуется изменить геном многочисленных клеток уже сформировавшегося организма, а не одной лишь яйцеклетки-зародыша. Для этого предлагается использовать вирусные частицы в качестве вектора. Вирусные частицы способны проникать в значительный процент клеток взрослого человека, встраивая в них свою наследственную информацию; возможно контролируемое размножение вирусных частиц в организме. При этом для уменьшения побочных эффектов учёные стараются избегать внедрения генно-инженерных ДНК в клетки половых органов, тем самым избегая воздействия на будущих потомков пациента. Также стоит отметить значительную критику этой технологии в СМИ: разработка генно-инженерных вирусов воспринимается многими как угроза для всего человечества.
С помощью генотерапии в будущем возможно изменение генома человека. В настоящее время эффективные методы изменения генома человека находятся на стадии разработки и испытаний на приматах. Долгое время генетическая инженерия обезьян сталкивалась с серьёзными трудностями, однако в 2009 году эксперименты увенчались успехом: в журнале Nature появилась публикация об успешном применении генно-инженерных вирусных векторов для исцеления взрослого самца обезьяны от дальтонизма. В этом же году дал потомство первый генетически модифицированный примат (выращенный из модифицированной яйцеклетки) - игрунка обыкновенная.
Хотя и в небольшом масштабе, генная инженерия уже используется для того, чтобы дать шанс забеременеть женщинам с некоторыми разновидностями бесплодия/ Для этого используют яйцеклетки здоровой женщины. Ребёнок в результате наследует генотип от одного отца и двух матерей.
Однако возможность внесения более значительных изменений в геном человека сталкивается с рядом серьёзных этических проблем.
Заключение
В результате интенсивного развития методов генетической инженерии получены клоны множества генов рибосомальной, транспортной и 5S РНК, гистонов, глобина мыши, кролика, человека, коллагена, овальбумина, инсулина человека и др. пептидных гормонов, интерферона человека и прочее.
Это позволило создавать штаммы бактерий, производящих многие биологически активные вещества, используемые в медицине, сельском хозяйстве и микробиологической промышленности.
На основе генетической инженерии возникла отрасль фармацевтической промышленности, названная «индустрией ДНК». Это одна из современных ветвей биотехнологии.
Для лечебного применения допущен инсулин человека (хумулин), полученный посредством рекДНК. Кроме того, на основе многочисленных мутантов по отдельным генам, получаемых при их изучении, созданы высокоэффективные тест-системы для выявления генетической активности факторов среды, в том числе для выявления канцерогенных соединений.
ИСПОЛЬЗОВАННАЯ ЛИТЕРАТУРА:
1) Бекиш О.-Я.Л. Медицинская биология. – Мн.: Ураджай, 2000. – с.114-119.
2) Мутовин Г.Р. Основы клинической генетики. – М.: Высшая школа, 1997. – с. 83-84.
3) Заяц Р.С. Основы медицинской генетики. – Мн.: Высшая школа, 1998. – с. 60-65.
4) biotechnolog.ru
План:
Введение.
1.Сущность генетической инженерии.
1.1. История генной инженерии
1.2. Понятие о генной инженерии
1.3. Цели и задачи генной инженерии
2. Этапы создания организмов с генетически измененной программой.
2.1. Выделение генов (естественных или синтезированных), содержащих необходимую информацию.
2.2. Подбор векторов (вирусы, плазмиды), способных к самостоятельной репликации в клетке реципиента.
2.3. Получение рекомбинантной ДНК.
2.4. Введение рекомбинантной ДНК в клетку - реципиент.
3.Применение генно-инженерных технологий в медицине.
Генетическая инженерия
Современная биология коренным образом отличается от традиционной биологии не только большей глубиной разработки познавательных идей, но и более тесной связью с жизнью общества, с прак- тикой. Можно сказать, что в наше время биология стала средством преобразования живого мира с целью удовлетворения материальных потребностей общества. Это заключение иллюстрируется прежде всего тесной связью биологии с биотехнологией, которая стала важнейшей областью материального производства, равноправным партнером механической и химической технологий, созданных чело- веком, а также с медициной.
С момента своего возникновения биология и биотехнология всегда развивались совместно, причем с самого начала биология была научной основой биотехнологии. Однако длительное время недостаток собственных данных не позволял биологии оказывать очень большое влияние на биотехнологию. Положение резко изменилось с созданием во второй половине XX в. методологии генетической инженерии, под которой понимают генетическое манипулирование с целью конструкции новых и реконструкции существующих генотипов. Являясь по своей природе методическим достижением, генетическая инженерия не привела к ломке сложившихся представлений о биологических явлениях, не затронула основных положений биологии подобно тому, как радиоастрономия не поколебала основных положений астрофизики, установление «механического эквивалента тепла» не привело к изменению законов теплопроводности, а доказательство атомистической теории вещества не изме- нило соотношений термодинамики, гидродинамики и теории упругости (А.А. Баев).
Тем не менее генетическая инженерия открыла новую эру в биологии по той причине, что появились новые возможности для про- никновения в глубь биологических явлений с целью дальнейшей характеристики форм существования живой материи, более эффективного изучения структуры и функции генов на молекулярном уровне, понимания тонких механизмов работы генетического аппарата. Успехи генетической инженерии означают переворот в современном
естествознании. Они определяют критерии ценности современных представлений о структурно-функциональных особенностях молекулярного и клеточного уровней живой материи. Современные данные о живом имеют гигантское познавательное значение, ибо обеспечивают понимание одной из важнейших сторон органического мира и тем самым вносят неоценимый вклад в создание научной картины мира. Таким образом, резко расширив свою познавательную базу, биология через генетическую инженерию оказала также ведущее влияние на подъем биотехнологии.
Генетическая инженерия создает заделы на пути познания способов и путей «конструирования» новых или улучшения существующих организмов, придавая им большую хозяйственную ценность и способность резкого увеличения продуктивности биотехнологических процессов. Однако генетическая инженерия создала новые горизонты и для медицины по линии диагностики и лечения многих болезней, как ненаследственных, так и наследственных. Она открыла новые пути в поисках новых лекарств и материалов, используемых в медицине. Генетическая инженерия и биотехнология стимулировали разработку методов бионанотехнологии.
В рамках генетической инженерии различают генную и клеточную инженерию. Под генной инженерией понимают манипуляции с целью создания рекомбинантных молекул ДНК. Часто эту методологию называют молекулярным клонированием, клонированием генов, технологией рекомбинантных ДНК или просто генетическими манипуляциями. Важно подчеркнуть, что объектом генной инженерии являются молекулы ДНК, отдельные гены. Напротив, под клеточной инженерией понимают генетические манипуляции с изолированными отдельными клетками или группами клеток растений и животных.
ГЕННАЯ ИНЖЕНЕРИЯ И ЕЕ ИНСТРУМЕНТЫ
Генную инженерию составляет совокупность различных экспериментальных приемов (методик), обеспечивающих конструкцию (реконструкцию), клонирование молекул ДНК и генов с заданными целями.
Методы генной инженерии используют в определенной последовательности (рис. 127), причем различают несколько стадий в выпол-
нении типичного генно-инженерного эксперимента, направленного на клонирование какого-либо гена, а именно:
1. Выделение плазмидий ДНК из клеток интересующего организма (исходного) и выделение ДНК-вектора.
2. Разрезание (рестрикция) ДНК исходного организма на фрагменты, содержащие интересующие гены, с помощью одного из ферментов-рестриктаз и выделение этих генов из рестрикционной смеси. Одновременно разрезают (рестрицируют) векторную ДНК, превращая ее из кольцевой структуры в линейную.
3. Смыкание интересующего сегмента ДНК (гена) с ДНК вектора с целью получения гибридных молекул ДНК.
4. Введение рекомбинантных молекул ДНК путем трансформации в какой-либо другой организм, например в Е. coli или соматические клетки.
5. Высев бактерий, в которые вводили гибридные молекулы ДНК, на питательные среды, позволяющие рост только клеток, содержащих гибридные молекулы ДНК.
6. Идентификация колоний, состоящих из бактерий, содержащих гибридные молекулы ДНК.
7. Выделение клонированной ДНК (клонированных генов) и ее характеристика, включая секвентирование азотистых оснований в клонированном фрагменте ДНК.
Рис. 127. Последовательные стадии генно-инженерного эксперимента
В ходе эволюции бактерии развили способность синтезировать так называемые рестрицирующие ферменты (эндонуклеазы), которые стали частью клеточной (бактериальной) системы рестрикциимодификации. У бактерий системы рестрикции-модификации являются внутриклеточной иммунной системой защиты от чужеродной ДНК. В отличие от высших организмов, у которых распознание и разрушение вирусов, бактерий и других патогенов происходит внеклеточно, у бактерий защита от чужеродной ДНК (ДНК растений и животных, в организме которых они обитают) происходит внутриклеточно, т.е. тогда, когда чужеродная ДНК проникает в цитоплазму бактерий. С целью защиты бактерии в ходе эволюции развили также способность «метить» собственную ДНК метилирующими основаниями на определенных последовательностях. По этой же причине чужеродная ДНК из-за отсутствия в ней метильных групп на тех же последовательностях плавится (разрезается) на фрагменты разными бактериальными рестриктазами, а затем деградируется бактериальными экзонуклеазами до нулеотидов. Можно сказать, что таким образом бактерии защи- щают себя от ДНК растений и животных, в организме которых они обитают временно (как патогены) или постоянно (как сапрофиты).
Рестриктазы впервые были выделены из Е. coli в 1968 г. Оказалось, что они способны разрезать (плавить) молекулы ДНК на разных сайтах (местах) рестрикции. Эти ферменты получили название эндонуклеаз класса I. Затем у бактерий были обнаружены эндонуклеазы класса II, которые распознают в чужеродной ДНК сайты рестрикции специфически и на этих сайтах тоже осуществляют рестрикцию. Именно ферменты этого класса стали использовать в генной инже- нерии. Тогда же были открыты ферменты класса III, которые плавят ДНК рядом с сайтами распознания, но эти ферменты не имеют значения в генной инженерии.
Действие системы рестрикции-модификации «рационализуется» так называемыми палиндромными (распознающими) последователь- ностями азотистых оснований, которые являются сайтами рестрикции ДНК. Палиндромные последовательности - это последовательности оснований, которые одинаково читаются вперед и назад, как, например, последовательность букв радар. Поскольку цепи ДНК обладают антипараллельным направлением, то считают, что последовательность является палиндромной, если она идентична, когда читается в направлении от 5" - к 3"-концу на верхней и на нижней цепи от 3" - к 5"-концу, а именно:

Палиндромы могут быть любых размеров, но большинство тех палиндромов, которые используют в качестве сайтов узнавания рестриктазами, состоят из 4, 5, 6 и реже 8 оснований.
Рестриктазы - это абсолютно необходимый инструмент в генной инженерии для вырезания интересующих фрагментов (генов) из больших молекул ДНК. Поскольку известно более 100 ферментов рестрикции, то это позволяет выбор рестриктаз и селективное вырезание фрагментов из исходной ДНК.
Замечательной особенностью рестриктаз является то, что они продуцируют разрезы молекул на несколько фрагментов (рестриктов) ДНК уступами, в результате чего в образующихся концах одна цепь длиннее другой, образуя своеобразный хвост. Такие концы (хвосты) получили название «липких» концов, так как они способны к самокомплементарности.
Рассмотрим результаты рестрикции на примере одной из наиболее известных рестриктаз Eco RI из системы рестрикция-модификация Е. соИ. Вместо того чтобы плавить ДНК в центре палиндромной последовательности узнавания, этот фермент плавит ДНК за преде- лами центра и продуцирует 4 самокомплементарных («липких») конца, состоящих из разного количества нуклеотидов, а именно:

Эти «липкие» концы в генно-инженерных опытах полезны по той причине, что они могут быть воссоединены комплементарно при низких температурах, что позволяет эффективное смыкание ДНК-фрагментов.
Сайты распознавания и сайты плавления в случае других рестриктаз имеют другое содержание, а именно:

Вслед за рестрикцией ДНК из рестрикционной смеси выделяют рестрикционные ДНК-фрагменты (ДНК-рестрикты), которые необ- ходимы затем для объединения с вектором. Для выделения ДНКрестриктов прибегают к электрофорезу, поскольку с помощью этого метода рестрикцированную ДНК очень легко фракционировать благодаря размерам фрагментов-рестриктов и константным отношениям электрический заряд-масса. Фрагменты в электрическом поле мигрируют в ходе электрофореза при частоте, зависимой от их размеров (массы). Чем больше (длиннее) фрагмент, тем медленнее он мигрирует в электрическом поле. Материалом, в котором проводят электрофорез, являются незаряжающиеся агароза или полиакриламид. Для опознания фрагментов используют этидий бромид, который красит фрагменты, что ведет к их более легкому обнаружению.
Результативность электрофореза очень высока, поскольку с его помощью могут быть разделены фрагменты, размеры которых состав- ляют от 2 до 50 000 оснований.
После электрофореза фрагменты из агарозы выделяют с помощью разных методов. На основании результатов сравнения размеров
рестриктов одной и той же ДНК, полученных с помощью разных рестриктаз, строят рестрикционные карты, на которых показывают сайты рестрикции каждой из использованных рестриктаз. В практическом плане рестрикционные карты позволяют определять не только размеры рестриктов, но и выяснять расположение в молекулах ДНК локусов тех или иных генов.
Поскольку у высших организмов в ходе транскрипции синтезируется гетерогенная ДНК, корректируемая процессингом, то в генной инженерии обычно используют комплементарную ДНК (кДНК), которую получают при использовании в качестве матрицы мРНК, на которой обратная транскриптаза синтезирует одноцепочечную ДНК (кДНК), являющуюся копией мРНК. В последующем эти одноцепочечные ДНК превращают в двухцепочечные ДНК. Считают, что кДНК содержит непрерывные нуклеотидные последовательности (транскрибируемые и транслируемые). Именно кДНК используют для рестрикции.
Выделенные после электрофореза из агарозных гелей фрагменты ДНК (рестрикты) можно предварительно подвергнуть сек-вентированию, т.е. определить в них нуклеотидную последовательность. Для этого служат химический и ферментативный методы секвентирования. Химический метод основан на получении меченных радиоактивным фосфором (32 Р) фрагментов и удалении из этих фрагментов одного из оснований с последующим учетом результатов радиоавтографии гелей, содержащих эти фрагменты. Ферментативный метод основан на том, что в конец анализируемого фрагмента вводят нуклеотид, используемый затем в синтезе разных фрагментов in vitro, анализируемых на нуклеотидную последовательность электрофоретически. Для изучения специфических последовательностей нуклеотидов в молекуле ДНК используют
также гибридизацию ДНК-ДНК, РНК-РНК, ДНК-РНК, Нозерн-
и Саузерен-блоттинги.
Генетические векторы. Сегмент ДНК (ген), который предназначен для молекулярного клонирования, должен обладать способностью к репликации при переносе его в бактериальную клетку, т.е. быть репликоном. Однако он такой способностью не обладает. Поэтому, чтобы обеспечить перенос и обнаружение клонируемых генов в клетках, их объединяют с так называемыми генетическими векторами. Последние должны обладать как минимум двумя свойствами. Во-первых, векторы должны быть способны к репликации
в клетках, причем в нескольких концах. Во-вторых, они должны обеспечивать возможность селекции клеток, содержащих вектор, т.е. обладать маркером, на который можно вести контрселекцию клеток, содержащих вектор вместе с клонируемым геном (рекомбинантные молекулы ДНК). Таким требованиям отвечают плазмиды и фаги. Плазмиды являются хорошими векторами по той причине, что они являются репликонами и могут содержать гены резистентности к какому-либо антибиотику, что позволяет вести селекцию бактерий на устойчивость к этому антибиотику и, следовательно, легкое обнаружение рекомбинантных молекул ДНК
(рис. 128).
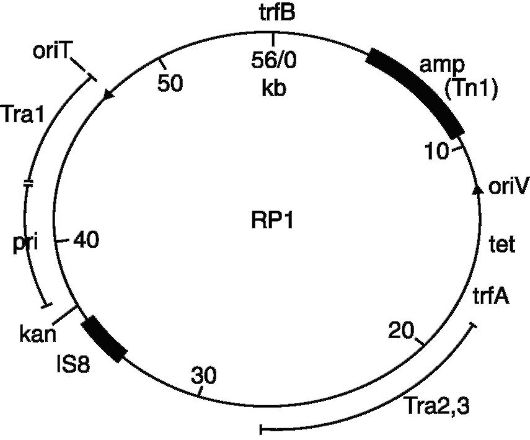
Рис. 128. Вектор pBRl
Поскольку не существует природных плазмидных векторов, то все известные к настоящему времени плазмидные векторы были сконструированы искусственно. Исходным материалом для создания ряда генетических векторов послужили R-плазмиды, в которых с помощью рестриктаз удаляли излишние последовательности ДНК, в том числе те, на которых располагались множественные сайты рестрикции. Это удаление определялось тем, что плазмидный вектор должен обладать только одним сайтом узнавания для одной рестриктазы, причем этот сайт должен лежать в функционально несущественном районе плазмидного генома. Например, плазмидый вектор pBR 322, который имеет гены резистентности к ампициллину и тетрациклину, что делает его очень удобным
для селекции бактерий, содержащих клонируемый сегмент ДНК, обладает одиночными сайтами рестрикции для более 20 ферментов- рестриктаз, включая такие известные рестриктазы, как Eco RI, Hind III, Pst I, Pva II и Sal I.
Фаговые векторы тоже обладают рядом преимуществ. Они могут включать в себя более крупные (более длинные) клонируемые фрагменты ДНК по сравнению с плазменными векторами. Далее, перенос фагами клонируемого фрагмента в клетки в результате инфицирования ими последних является более эффективным, чем трансформация ДНК. Наконец, фаговые векторы позволяют более эффективный скрининг (распознание) на поверхности агара колоний, содержащих клетки, несущие клонируемый ген. Многие фаговые векторы сконструированы на базе фага лямбда.
Кроме фаговых используют и другие вирусные векторы, сконструированные на базе вируса герпеса, а также векторы, сконструированные на базе дрожжевой ДНК.
Если клонирование генов проводят, используя клетки млекопитающих или растений, то требования к векторам те же, что и в случае клонирования в бактериальных клетках.
Конструирование рекомбинантных молекул ДНК. Непосредственное конструирование рекомбинантных молекул ДНК следует после того, как получены рестрикты исследуемой ДНК и векторной ДНК. Оно заключается в смыкании сегментов-рестриктов исследуемой ДНК с рестриктом векторной ДНК, которая в результате рестрикции превращается из кольцевой в линейную ДНК.
Чтобы сомкнуть фрагменты исследуемой ДНК с ДНК вектора, используют ДНК-лигазу (рис. 129). Лигирование будет успешным, если смыкаемые структуры обладают З"-гидроксильной и 5"-фос- фатной группами и если эти группы расположены соответствующим образом относительно одна другой. Фрагменты объединяются через их «липкие» концы в результате самокомплементарности. При высоких концентрациях фрагментов последние время от времени становятся в правильное положение (напротив друг друга). Многие рестриктазы, такие как Eco RI, продуцируют «липкие» концы, состоящие из четырех оснований. Процесс лигирования «липких» концов, состоящих из четырех оснований, происходит при пониженной температуре (до 12 ?С).
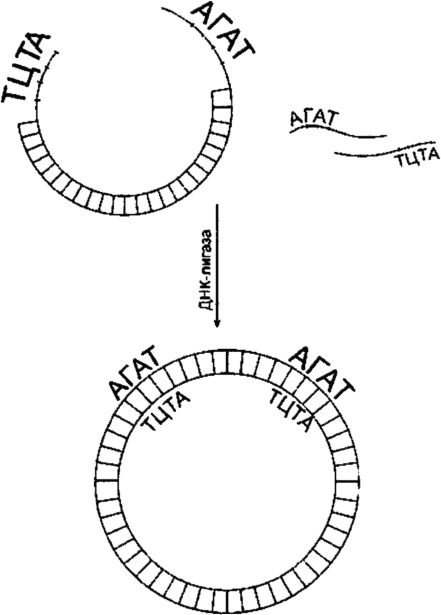
Рис. 129. ДНК-лигирование
Если при рестрикции образуются фрагменты без «липких» концов, то их «насильственно» конвертируют в молекулы с «липкими» концами, используя фермент трансферазу. Этот фермент добавляет нуклеотиды к 3"-концу ДНК. На одном фрагменте может быть добавлен поли-А-хвост, на другом - поли-Т-хвост. Для генерации любых желаемых концов ДНК используют также полимеразную цепную реакцию (ПЦР). Принцип ПЦР основан на денатурации выделенной из клеток ДНК и «отжиге» ее с добавлением к ренатурирующимся цепям ДНК-олигонуклеотидов, состоящих из 15-20 нуклеотидов каждый. Эти олигонуклеотиды должны быть комплементарны последовательностям в цепях, разделенных расстояниями в 50-2000 нуклеотидов. Будучи «затравкой» для синтеза ДНК in vitro, они позволяют ДНК-полимеразе копировать те участки, которые находятся между «затравками». Это копирование дает большое количество копий изучаемого фрагмента ДНК.
Введение рекомбинантных молекул ДНК в клетки. После смыкания интересующего фрагмента ДНК (гена) с генетическим вектором с помощью ДНК-лигазы образованные рекомбинантные молекулы вводят в клетки с целью добиться их репликации (за счет генетического вектора) и увеличения количества копий. Наиболее популярным способом введения в клетки рекомбинантных молекул ДНК, в которых вектором служит плазмида, является трансформация Е. coli. С этой целью бактериальные клетки предварительно обрабатывают кальцием или рубидием (ионами), для того
чтобы они стали «компетентными» в восприятии рекомбинатной ДНК. Чтобы повысить частоту проникновения ДНК в клетки, используют метод электропорации, заключающийся в кратком экспонировании клеток в интенсивном электрическом поле. Эта обработка создает полости в мембранах клеток, что способствует лучшему восприятию клетками ДНК. После введения рекомбинатных молекул ДНК в бактерии последние высевают на МПА (мясо-пептонный агар), обогащенный антибиотиками для селекции желаемых клеток, т.е. клеток, содержащих рекомбинантные молекулы ДНК. Частота трансформации является невысокой. Обычно один трансформант возникает на 10 5 высеянных клеток. Если же вектор является фаговым, то прибегают к трансфекции клеток (бактерий или дрожжей) фагом. Что касается соматических клеток животных, то их трансфекцию осуществляют ДНК в присутствии химических веществ, облегчающих прохождение ДНК через плазматические мембраны. Возможны также прямые микроинъекции ДНК в овоциты, в культивируемые соматические клетки и в эмбрионы млекопитающих.
Важнейшим моментом, связанным с молекулярным клонированием, является поиск способа, позволяющего установить, действитель- но ли клонируемый фрагмент включился в вектор и вместе с вектором, образовав рекомбинатную молекулу ДНК, вошел в клетки. Если речь идет о бактериальных клетках, то один из способов основан на учете инсерционной инактивации плазмидного (векторного) гена резистентности. Например, в плазмидном векторе pBR 322, детерминирующем резистентность к ампициллину и тетрациклину, един- ственный сайт для рестриктазы Pst I находится в локусе, занимаемом геном резистентности к ампициллину. Pst I-плавление на этом сайте генерирует «липкие» концы, позволяющие лигирование клонируемого фрагмента с векторной ДНК. Однако при этом плазмидный (векторный) ген ампициллинрезистентности инактивируется, тогда как ген тетрациклинрезистентности на векторе остается интактным. Именно ген тетрациклинрезистентности и используется для селекции клеток, трансформируемых рекомбинантными молекулами ДНК. Это позволяет убедиться, что клетки выросших колоний на среде с тетрациклином действительно содержат рекомбинантные молекулы ДНК, их проверяют с помощью так называемого «спот-теста» на паре чашек с плотной средой, одна из которых содержит ампициллин, тогда как другая лишена этого антибиотика. Клонируемые ДНК находятся
лишь в трансформантах, резистентных к тетрациклину. Что касается трансформантов, резистентных одновременно к ампициллину и тетрациклину (АрТс), то они содержат плазмидные (векторные) молекулы, которые спонтанно приобрели кольцевую форму без включения в них чужеродной (клонируемой) ДНК.
Другой способ обнаружения инсерции чужеродных (клонируемых) фрагментов в плазмидный вектор основан на использовании вектора, содержащего ген β-галактозидазы. Инсерция чужеродной ДНК в этот ген неизбежно инактивирует синтез β-галактозидазы, что может быть обнаружено посевом трансформированных клеток на среду, которая содержит субстраты β-галактозидазы. Эта среда позволяет селекцию окрашенных колоний клеток. Существуют и другие методы.
Как уже отмечено, рестрикционные линейные фрагменты векторной ДНК способны к восстановлению кольцевой структуры без включения в них клонируемых сегментов. Чтобы уменьшить частоту спонтанного образования таких кольцевых молекул векторной ДНК, рестрикты векторной ДНК обрабатывают фосфатазой. В результате этого образование кольцевых молекул ДНК становится невозможным, поскольку будут отсутствовать концы 5"-РО 4 , необходимые для действия лигазы.
Совокупность колоний-трансформантов, выросших на селективной среде, представляет собой совокупность клеток, содержащих клоны разных фрагментов (генов) клонируемой геномной или кДНК. Коллекции этих клонов формируют так называемые библиотеки ДНК, широко используемые в генно-инженерных работах.
Заключительной стадией клонирования генов является выделение и исследование клонированной ДНК, включая секвенирование. Перспективные штаммы бактерий или соматических клеток, содержащих рекомбинантные молекулы ДНК, которые контролируют синтез интересующих белков, имеющих коммерческую ценность, передают в промышленность.
КЛЕТОЧНАЯ ИНЖЕНЕРИЯ
Как отмечено в начале главы, клеточной инженерией называют генетические манипуляции с изолированными клетками животных и растений. Эти манипуляции часто осуществляют in vitro, а главной целью они имеют получение генотипов этих организмов с заданными свойствами, в первую очередь хозяйственно полезными. Что касает-
ся человека, то клеточная инженерия оказалась применимой к его половым клеткам.
Предпосылкой к развитию клеточной инженерии у человека и животных явилась разработка методов культивирования их сома- тических клеток на искусственных питательных средах, а также получение гибридов соматических клеток, включая межвидовые гибриды. В свою очередь успехи в культивировании соматических клеток оказали влияние на изучение половых клеток и оплодотворения у человека и животных. Начиная с 60-х гг. ХХ в. в нескольких лабораториях мира были выполнены многочисленные эксперименты по пересадке ядер соматических клеток в яйцеклетки, искусственно лишенные ядер. Результаты этих экспериментов часто были противоречивы, но в целом они привели к открытию способности клеточных ядер обеспечивать нормальное развитие яйцеклетки (см. гл. IV).
На основе результатов изучения развития оплодотворенных яйцеклеток в 60-е гг. XX в. были начаты также исследования по выяснению возможности оплодотворения яйцеклеток вне организма матери. Очень быстро эти исследования привели к открытию возможности оплодотворения яйцеклеток сперматозоидами в пробирке и дальнейшего развития образованных таким путем зародышей при имплантации в матку женщины. Дальнейшее совершенствование разработанных в этой области методов привело к тому, что рождение «пробирочных» детей стало реальностью. Уже к 1981 г. в мире было рождено 12 детей, жизнь которым была дана в лаборатории, в пробирке. В настоящее время этот раздел клеточной инженерии получил большое распространение, а количество «пробирочных» детей составляет уже десятки тысяч (рис. 130). В России работы по получению «пробирочных» детей были начаты только в 1986 г.
В 1993 г. была разработана методика получения монозиготных близнецов человека in vitro путем разделения эмбрионов на бласто- меры и доращивания последних до 32 клеток, после чего они могли быть имплантированы в матку женщины.
Под влиянием результатов, связанных с получением «пробирочных» детей, у животных тоже была разработана технология, получившая название трансплантации эмбрионов. Она связана с разработкой способа индукции полиовуляции, способов искусственного оплодот- ворения яйцеклеток и имплантации зародышей в организм животных - приемных матерей. Суть этой технологии сводится к следую-
щему. Высокопродуктивной корове вводят гормоны, в результате чего наступает полиовуляция, заключающаяся в созревании сразу 10-20 клеток. Затем яйцеклетки искусственно оплодотворяются мужскими половыми клетками в яйцеводе. На 7-8-й день зародыши вымывают из матки и трансплантируют в матки другим коровам (приемным матерям), которые затем дают жизнь телятам-близнецам. Телята наследуют генетический статус своих подлинных родителей.

Рис. 130. «Пробирочные» дети
Другой областью клеточной инженерии у животных является создание трансгенных животных. Наиболее простой способ получения таких животных заключается во введении в яйцеклетки исходных животных линейных молекул ДНК. Животные, развившиеся из оплодотворенных таким образом яйцеклеток, будут содержать в одной из своих хромосом копию введенного гена и, кроме того, они будут передавать этот ген по наследству. Более сложный способ получения трансгенных животных разработан на мышах, различающихся по окраске шерстного покрова, и сводится к следующему. Вначале из организма беременной серой мыши извлекают четырехдневных зародышей и измельчают их на отдельные клетки. Затем из эмбриональных клеток извлекают ядра, переносят их в яйцеклетки черных мышей, предварительно лишенных ядер. Яйцеклетки черных мышей, содержащие чужие ядра, помещают в пробирки
с питательным раствором для дальнейшего развития. Развившиеся из яйцеклетки черных мышей зародыши имплантируют в матки белых мышей. Таким образом, в этих экспериментах удалось получить клон мышей с серой окраской шерстного покрова, т.е. клонировать эмбриональные клетки с заданными свойствами. В главе IV мы рассмотрели результаты оплодотворения искусственно лишенных ядер яйцеклеток овец ядерным материалом соматических клеток животных этого же вида. В частности, из яйцеклеток овец удаляли ядра, а затем в такие яйцеклетки вводили ядра соматических клеток (эмбриональных, плодовых или клеток взрослых животных), после чего оплодотворенные таким образом яйцеклетки вводили в матки взрослых овец. Рождающиеся ягнята оказались идентичными овцедонору. Пример - овца Долли. Получены также клоновые телята, мыши, кролики, кошки, мулы и другие животные. Такое конструирование трансгенных животных представляет собой прямой путь клонирования животных с хозяйственно полезными признаками, включая особей определенного пола.
Трансгенные животные получены также при использовании исходного материала, принадлежащего разным видам. В частности, известен способ передачи гена, контролирующего гормон роста, от крыс в яйцеклетки мышей, а также способ комбинирования бластомеров овцы с бластомерами козы, что привело к возникновению гибридных животных (ковец). Эти эксперименты указывают на воз- можность преодоления видовой несовместимости на самых ранних этапах развития. Особенно заманчивые перспективы открываются (если видовая несовместимость будет преодолена полностью) на пути оплодотворения яйцеклеток одного вида ядрами соматических клеток другого вида. Речь идет о реальной перспективе создания хозяйственно ценных гибридов животных, которых невозможно получить путем скрещиваний.
Следует отметить, что ядерно-трансплантационные работы еще не очень эффективны. Эксперименты, выполненные на земноводных и млекопитающих, в целом показали, что их результативность является небольшой, причем она зависит от несовместимости между донорскими ядрами и реципиентными овоцитами. Кроме того, препятствием на пути к успехам являются также образующиеся хромосомные аберрации в трансплантированных ядрах в ходе даль- нейшего развития, которые сопровождаются гибелью трансгенных животных.
На стыке работ по изучению гибридизации клеток и иммунологических исследований возникла проблема, связанная с получением и изучением так называемых моноклональных антител. Как отмечено выше, антитела, продуцируемые организмом в ответ на введение антигена (бактерии, вирусы, эритроциты и т.д.), представляют собой белки, называемые иммуноглобулинами и составляющие фундаментальную часть защитной системы организма против возбудителей болезней. Но любое чужеродное тело, вводимое в организм, представляет собой смесь разных антигенов, которые будут возбуждать продукцию разных антител. Например, эритроциты человека обладают антигенами не только для групп крови А (II) и В (III), но и многими другими антигенами, включая резус-фактор. Далее, белки клеточной стенки бактерий или капсида вирусов также могут действовать в качестве разных антигенов, вызывающих образование разных антител. В то же время лимфоидные клетки иммунной системы организма обычно представлены клонами. Значит, даже только по этой причине в сыворотке крови иммунизированных животных антитела всегда представляют собой смесь, состоящую из антител, продуцируемых клетками разных клонов. Между тем для практических потребностей необходимы антитела только одного типа, т.е. так называемые моноспецифические сыворотки, содержащие антитела только одного типа или, как их называют, моноклональные антитела.
В поисках методов получения моноклональных антител швейцарскими исследователями в 1975 г. был открыт способ гибридизации между лимфоцитами мышей, иммунизированных тем или иным антигеном, и культивируемыми опухолевыми клетками костного мозга. Такие гибриды получили название «гибри- домные». От «лимфоцитарной» части, представленной лимфоцитом одного клона, одиночная гибридома наследует способность вызывать образование необходимых антител, причем одного типа, а благодаря «опухолевой (миэломной)» части она становится способной, как и все опухолевые клетки, бесконечно долго размно- жаться на искусственных питательных средах, давая многочисленную популяцию гибридов. На рис. 131 показана схема выделения клеточных линий, синтезирующих моноклональные антитела. Линии мышиных клеток, синтезирующих моноклональные антитела, выделяют путем слияния миеломных клеток с лимфоцитами из селезенки мыши, иммунизированной за пять дней до этого
желаемым антигеном. Слияния клеток достигают смешиванием их в присутствии полиэтиленгликоля, который индуцирует слияние клеточных мембран, а затем в высеве их на питательную среду, позволяющую рост и размножение только гибридных клеток (гибридом). Размножение гибридом проводят в жидкой среде, где они растут далее и секретируют антитела в культуральную жидкость, причем только одного типа, к тому же в неограниченных количествах. Эти антитела получили название моноклональных. Чтобы повысить частоту образования антител, прибегают к клонированию гибридом, т.е. к селекции отдельных колоний гибридом, способных вызывать образование наибольшего количе- ства антител желаемого типа. Моноклональные антитела нашли широкое применение в медицине для диагностики и лечения ряда болезней. В то же время важнейшее преимущество моноклональной технологии заключается в том, что с ее помощью могут быть получены антитела против материалов, которые невозможно очистить. Напротив, можно получить моноклональные антитела против клеточных (плазматических) мембран нейронов животных. Для этого мышей иммунизируют выделенными мембранами нейронов, после чего их селезеночные лимфоциты объединяют с миеломными клетками, а дальше поступают, как описано выше.

Рис. 131. Получение моноклональных антител
ГЕНЕТИЧЕСКАЯ ИНЖЕНЕРИЯ И МЕДИЦИНА
Генная инженерия оказалась очень перспективной для медицины, прежде всего в создании новых технологий получения физиологически активных белков, используемых в качестве лекарств (инсулин, соматостатин, интерфероны, соматотропин и др.).
Инсулин используют для лечения больных диабетом, который стоит на третьем месте (после болезней сердца и рака) по частоте вызываемых смертельных случаев. Мировая потребность инсулина составляет несколько десятков килограммов. Традиционно его получают из панкреатических желез свиней и коров, но гормоны этих животных слегка отличаются от инсулина человека. Инсулин свиней различается по одной аминокислоте, а коровий - по трем. Считают, что инсулин животных часто вызывает побочные эффекты. Хотя химический синтез инсулина осуществлен давно, но до сих пор промышленное производство гормонов оставалось очень дорогим. Сейчас получают дешевый инсулин с помощью генно-инженерного метода путем химико-ферментативного синтеза гена инсулина с последующим введением этого гена в кишечную палочку, которая затем синтезирует гормон. Такой инсулин более «биологичен», так как химически идентичен инсулину, вырабатываемому клетками поджелудочной железы человека.
Интерфероны - белки, синтезируемые клетками главным образом в ответ на заражение организма вирусами. Интерфероны характери- зуются видовой специфичностью. Например, у человека установлены три группы интерферонов, продуцируемых различными клетками под контролем соответствующих генов. Интерес к интерферонам определяется тем, что их широко используют в клинической практике для лечения многих болезней человека, особенно вирусных.
Имея крупные размеры, молекулы интерферона мало доступны для синтеза. Поэтому большинство интерферонов сейчас получают из крови человека, но выход при таком способе получения небольшой. Между тем потребности в интерфероне исключительно велики. Это поставило задачу изыскать эффективный метод производства интерферона в промышленных количествах. Генетическая инженерия лежит в основе современного производства «бактериального» интерферона.
Усилилось влияние генетической инженерии на технологию тех лекарственных веществ, которые уже давно создаются по био- логической технологии. Еще в 40-50-е гг. XX в. была создана
биологическая промышленность для производства антибиотиков, которые составляют наиболее эффективную часть лекарственного арсенала современной медицины. Однако в последние годы отмечается значительный рост лекарственной устойчивости бактерий, особенно к антибиотикам. Причина заключается в широком распространении в микробном мире плазмид, детерминирующих лекарственную устойчивость бактерий. Именно поэтому многие знаменитые ранее антибиотики утратили свою былую эффективность. Единственный пока путь преодоления резистентности бактерий к антибиотикам - это поиски новых антибиотиков. По оценкам специалистов, в мире ежегодно создают около 300 новых антибиотиков. Однако большинство из них либо неэффективно, либо токсично. В практику же каждый год вводится лишь несколько антибиотиков, что заставляет не только сохранять, но и увеличивать мощность антибиотической промышленности на основе генно-инженерных разработок.
Основные задачи генной инженерии в тех технологиях лекарственных веществ, в которых продуцентами лекарств являются микроорганизмы, определяются необходимостью генно-инженерной реконструкции последних с целью повышения их активности. В то же
время началась реализация идеи создания лекарств в виде малых молекул, что способствует их большей эффективности.
Иммунная биотехнология связана с производством прежде всего вакцин нового поколения для профилактики инфекционных болезней человека и животных. Первыми коммерческими продуктами, созданными с помощью генетической инженерии, стали вакцины против гепатита людей, ящура животных и некоторые другие. Исключительно важное направление в этой области связано с производством моноклональных антител, реагентов, необходимых для диа- гностики возбудителей болезни, а также для очистки гормонов, витаминов, белков различной природы (ферментов, токсинов и др.).
Значительный практический интерес представляет метод получения искусственного гемоглобина путем введения гемоглобиновых генов в растения табака, где под контролем этих генов продуциру- ются α- и β-цепи глобина, которые объединяются в гемоглобин. Синтезируемый в клетках табачных растений гемоглобин полностью функционален (связывает кислород). Клеточная инженерия в применении к человеку связана не только с решением фундаментальных проблем биологии человека, но и с преодолением прежде всего женского бесплодия. Поскольку частота положительных случаев имплантации в матку женщин эмбрионов, полученных in vitro, является небольшой, то получение монозиготных близнецовэмбрионов in vitro также имеет значение, так как увеличиваются возможности повторных имплантаций за счет «запасных» эмбрионов. Особый интерес представляют перспективы использования стволовых клеток в качестве источника замены клеток и тканей в лечении таких болезней, как диабет, повреждения спинного мозга, боли сердца, остиоартриты, болезнь Паркинсона. Но для реализации этих перспектив необходимо углубленное изучение биологии стволовых клеток.
В использовании генетической инженерии применительно к проблемам медицины особое значение приобрела задача разработки генно-инженерных методов радикального лечения наследственных болезней, которые, к сожалению, еще не поддаются лечению существующими методами. Содержание этой задачи заключается в разработке способов исправления (нормализации) мутаций, результатом которых являются наследственные болезни, и в обеспечении передачи «исправлений» по наследству. Считают, что успешной разработке генно-инженерных методов лечения наследственных болезней будут
способствовать данные о геноме человека, полученные в результате выполнения международной научной программы «Геном человека».
ЭКОЛОГИЧЕСКИЕ ПРОБЛЕМЫ ГЕНЕТИЧЕСКОЙ ИНЖЕНЕРИИ
Подняв на новый уровень биотехнологию, генетическая инженерия нашла также применение в разработке способов определения и устранения загрязнений окружающей среды. В частности, сконструированы штаммы бактерий, которые являются своеобразными индикаторами мутагенной активности химических загрязнений. С другой стороны, генно-инженерным способом сконструированы штаммы бактерий, содержащие плазмиды, под контролем которых происходит синтез ферментов, способных разрушать многие химические соединения- загрязнители среды обитания. В частности, некоторые плазмидосодержащие бактерии способны разлагать до безвредных соединений нефть и нефтепродукты, оказавшиеся в среде в результате различных аварий или других неблагоприятных причин.
Однако генетическая инженерия - это превращение генетического материала, которое в природе отсутствует. Следовательно, продукты генной инженерии - это абсолютно новые продукты, не существующие в природе. Поэтому она сама по себе из-за неизвестности ее продуктов таит опасность как для природы и среды обитания, так и для персонала, работающего в лабораториях, где используют методы генетической инженерии или работают со структурами, созданными в ходе генно-инженерных работ.
Поскольку возможности клонирования генов безграничны, то еще в самом начале этих исследований среди ученых возникли вопросы о природе создаваемых организмов. Одновременно были высказаны предположения о ряде нежелательных последствий этой методологии, причем эти предположения нашли поддержку и среди широкой общественности. В частности, появились раз- ногласия о свойствах бактерий, получивших в генно-инженерных экспериментах гены животных. Например, сохраняют ли бактерии Е. coli свою видовую принадлежность из-за содержания введенных в них генов животного происхождения (например, гена инсулина) или их следует считать новым видом? Далее, насколько долговечны такие бактерии, в каких экологических нишах они могут
существовать? Но самое главное стало заключаться в появлении опасений, что в ходе производства и манипуляций с рекомбинантными молекулами ДНК могут быть созданы генетические структуры со свойствами, непредвиденными и опасными для здоровья человека, для исторически сложившегося экологического равновесия. Тогда же начались и призывы к мораторию на генетическую инженерию. Эти призывы вызвали международный резонанс и привели к международной конференции, которая состоялась в 1975 г. в США и на которой широко обсуждались возможные последствия исследований в этой области. Затем в странах, где стала развиваться генетическая инженерия, были выработаны правила работы с рекомбинантными молекулами ДНК. Эти правила направлены на исключение попадания в среду обитания продуктов деятельности генно-инженерных лабораторий.
Другой аспект нежелательных последствий генно-инженерных работ связан с опасностью для здоровья персонала, работающего в лабораториях, где применяют методы генетической инженерии, поскольку в таких лабораториях используют фенол, этидий бромид, УФ-излучения, которые являются вредными для здоровья факторами. Кроме того, в этих лабораториях существует возможность заражения бактериями, содержащими рекомбинантные молекулы ДНК, контролирующие нежелательные свойства, например лекарственную резистентность бактерий. Эти и другие моменты определяют необходимость повышения уровня техники безопасности в генноинженерных работах.
Наконец, широко обсуждаются в обществе проблемы опасности генетически модифицированных продуктов (генетически изме- ненных томатов, картофеля, кукурузы, сои), а также таких продуктов, как хлеб, пасты, конфеты, мороженое, сыр, растительное масло, мясные продукты, которые в ряде стран, особенно в США, приобрели широкое распространение. На протяжении 12 000 лет сельского хозяйства человек употреблял продукты естественного происхождения. Поэтому предполагают, что с генетически модифицированной пищей в организм человека попадут новые токсины, аллергены, бактерии, канцерогены, что приведет к совершенно новым болезням будущих поколений. В связи с этим возникает вопрос о подлинно научной оценке генетически модифицированной пищи.
ВОПРОСЫ ДЛЯ ОБСУЖДЕНИЯ
1. Что понимают под генной, клеточной и генетической инженерией? Есть ли разница между этими понятиями и молекулярном клонировании?
2. В чем заключается прогрессивность генетической инженерии по сравнению с другими методами, используемыми в биологии?
3. Перечислите основные «инструменты» генной инженерии.
4. Что представляют собой ферменты-рестриктазы, каковы их свойства и их роль в генной инженерии?
5. Все ли рестриктазы образуют «липкие» концы исследуемых ДНК и зависит ли структура «липких» концов от вида рестриктазы?
6. Дайте определение генетическим векторам. Существуют ли природные векторы?
7. Как получают генетические векторы в лабораторных условиях? Какие биологические объекты являются исходным материалом для получения векторов?
8. Какова предельная длина последовательностей азотистых оснований ДНК, которые еще могут включиться в генетический вектор? Различаются ли векторы по «мощности»?
9. Охарактеризуйте свойства ДНК-лигазы и определите ее роль в генной инженерии.
10. Как смыкают клонируемый сегмент ДНК (ген) с генетическим вектором?
11. Какова частота введения рекомбинантных молекул ДНК в бактериальные клетки?
12. На каком принципе основана селекция бактериальных клеток, содержащих рекомбинантные молекулы ДНК? Приведите один из примеров такой селекции.
14. Многие штаммы бактерий обладают одинаковыми ферментами, практически одинаково обеспечивающими их метаболизм. Между тем нуклеотидная специфичность систем рестрикции-модификации бактерий различна. Можете ли вы объяснить это явление?
15. Почему последовательности ДНК, представляющие сайты распознавания рестриктазами, не могут содержать более восьми пар оснований?
16. Сколько раз последовательность ГГЦЦ, распознаваемая рестриктазой Нае III, будет встречаться в сегменте ДНК длиной в 50 000 пар оснований с 30-, 50- и 70-процентным содержанием ГЦ?
17. Рестриктазы Bam HI и Bgl I плавят последовательности Г ГАТЦЦ и Т ГАТЦА соответственно. Можно ли включить в сайт Bam HI фрагменты ДНК, продуцированные Bgl I-рестрикцией? Если да, то почему? Если используемая плазмида (вектор) содержит один сайт для рестрикции Bgl I, то на какой питательной среде можно осуществить селекцию бактерий, эту плазмиду?
18. Вычислите частоту трансформации бактерий на одну молекулу ДНК, если на 5000 плазмидных пар оснований образуется 5-10 5 трансформантов?
19. Можно ли клонировать 0-пункт репликации ДНК Е. coli и если да, то каким образом?
20. Можно ли определить, сколько необходимо молекул ДНК для трансформации одной клетки Е. coli?
21. Можно ли с помощью полимеразной цепной реакции определить сайт сплайсинга на мРНК?
22. Каким образом можно использовать полимеразную цепную реакцию для того, чтобы ввести желаемый сайт рестрикции в интересующее место на фрагменте ДНК, предназначенном для клонирования?
23. Назовите методы клеточной инженерии в применении к животным. Какова хозяйственная ценность животных, получаемых этими методами?
24. Дайте определение понятиям «трансгенные растения» и «трансгенные животные». Сохраняют ли трансгенные организмы свою видовую принадлежность или их можно считать организмами новых видов?
25. Что такое гибридомы и моноклональные антитела? Как их получают?
26. Применима ли клеточная инженерия к человеку?
27. Допустим, что инъекция чужеродной ДНК в яйцеклетку мыши и имплантация оплодотворенной таким путем яйцеклетки в организм мыши закончились ее беременностью и рождением мышат, содержащих в геноме копии инъецированной ДНК. Однако мышата оказались мозаиками, т.е. одни их клетки содержат копии инъецированной ДНК, другие лишены этой ДНК. Можете ли вы объяснить природу этого явления?
28. Считаете ли вы генетически опасной пищу, приготовленную из генетически измененных продуктов?
29. Необходима ли научная экспертиза генетически измененных продуктов питания?
Познание определяется тем, что утверждается нами как Истина.
П.А. Флоренский, 1923
Генетическая инженерия и современная биотехнология возникли в результате развития микробиологии, генетики и биохимии. Достижения молекулярной биологии, молекулярной генетики, биологии клетки, а также вновь открытые эксперимен-тальные методы и новое оборудование обеспечили немыслимые темпы развития генетической инженерии и биотехнологии.
Цель генной инженерии
Целью генной инженерии является изменение строения генов, их расположения в хромосоме и регулирование их деятельности в со-ответствии с потребностями человека. Для достижения этой цели применяются различные методы, позволяющие осуществлять в про-мышленных масштабах производство белков, создавать новые сорта растений и породы животных, наиболее отвечающие требованиям, диагностировать и лечить различные инфекционные и наследствен-ные болезни человека.
Объектами исследования генетической инженерии являются вирусы, бактерии, грибы , животные (в том числе организм человека) и растительные клетки. После очищения молекулы ДНК этих живых существ от других веществ клетки материальные различия между ними исчезают. Очищенная молекула ДНК может быть расщеплена с помощью энзимов на специфические отрезки, которые затем при необходимости можно с помощью сшивающих энзимов соединить между собой. Современные методы генетической инженерии позволяют размножать любой отрезок ДНК или заменять любой нуклеотид в цепи ДНК другим. Разумеется, эти успехи достигнуты в результате последовательного изучения закономерностей наследственности.
Генетическая инженерия (генная инженерия) возникла в результате открытия энзимов, специфическим образом разделяющих материальную основу наследственности — молекулу ДНК на отрезки и соединяющих эти отрезки концами друг с другом, а также электрофоретического метода, позволяющего с высокой точностью разделять по длине отрезки ДНК. Создание методов и оборудования для определения специфической последовательности нуклеотидов, образующих молекулу ДНК, а также для автоматического синтеза любого желаемого отрезка ДНК обеспечило развитие генетической инженерии быстрыми темпами.
Развитию у учёных стремления управлять наследст-венностью способствовали доказательства, свидетельствующие о том, что основу наследственности всех растений и животных составляет молекула ДНК, что бактерии и фаги также подчиняются законам наследст-венности, что мутационный процесс является общим для всех живых существ и может регулироваться экспериментальными методами.
Луи Пас-тер
Вели-кий французский учёный Луи Пас-тер, разработав метод получения клонов, первым показал, что бак-терии разнообразны, обладают нас-ледственностью и их свойства тесно связаны с последней (рис. 1, 2).
Туорт и Д’Эррель
В 1915 г. Туорт и Д’Эррель доказали, что фаги (фаги — вирусы, размножающиеся в бактериях), самопроизвольно размножаясь внутри бактерий, могут их уничтожить. Микробиологи возлагали надежды на использование фагов против микробов — возбудителей опасных инфекционных заболеваний. Однако бактерии обладают устойчивостью к фагам вследствие само-произвольных спонтанных мутаций. Наследование этих мутаций предохраняет бактерии от уничтожения со стороны фагов.
Размножаясь внутри клетки, вирусы и фаги могут погубить её или, внедрившись в геном клетки, изменить её наследственность. Для изменения наследственности организма широко используются процессы трансформации и трансдукции .
Джошуа и Эстер Ледерберги
В 1952 г. Джошуа и Эстер Ледерберги, используя метод копирования (репликации) колоний бактерий, до-казали существование самопроиз-вольных мутаций в бактериях (рис. 3). Они разработали метод, позволяющий выделять мутантные клетки с помощью репликации. Под влиянием внешней среды частота мутаций возрастает. Специальные методы позволяют увидеть невооружённым глазом клоны новых штаммов , образовавшихся в результате мутаций.
Метод репликации колоний бактерий осуществляется следующим образом. Стерилизованную бархатную ткань натягивают на поверхность деревянного приспособления и прик-ладывают к колонии бактерий, рас-тущих на поверхности чашки Петри, предназначенной для пересадки реп-лик. Затем колонии переносят в чистую чашку Петри с искусствен-ной питательной средой . Материал с сайта
Этапы генной инженерии
Генная инженерия осуществляется в несколько этапов.
- Определяют ген, представляющий интерес по его функциям, затем его выделяют, клонируют и изучают его структуру.
- Выделенный ген соединяют (рекомбинируют) с ДНК какого-нибудь фага, транспозона или плазмиды , имеющей способность рекомбинироваться с хромосомой, и таким путём создают век-торную конструкцию.
- Векторную конструкцию встраивают в клетку (транс¬формация) и получают трансгенную клетку.
- Из трансгенной клетки в искусственных условиях можно полу¬чить зрелые организмы.
Экономическое значение
Генная инженерия служит для получения желаемых качеств изменяемого или генетически модифицированного организма . В отличие от традиционной селекции , в ходе которой генотип подвергается изменениям лишь косвенно, генная инженерия позволяет непосредственно вмешиваться в генетический аппарат, применяя технику молекулярного клонирования . Примерами применения генной инженерии являются получение новых генетически модифицированных сортов зерновых культур, производство человеческого инсулина путём использования генномодифицированных бактерий, производство эритропоэтина в культуре клеток или новых пород экспериментальных мышей для научных исследований.
Основой микробиологической, биосинтетической промышленности является бактериальная клетка. Необходимые для промышленного производства клетки подбираются по определённым признакам, самый главный из которых - способность производить, синтезировать, при этом в максимально возможных количествах, определённое соединение - аминокислоту или антибиотик, стероидный гормон или органическую кислоту. Иногда надо иметь микроорганизм, способный, например, использовать в качестве «пищи» нефть или сточные воды и перерабатывать их в биомассу или даже вполне пригодный для кормовых добавок белок. Иногда нужны организмы, способные развиваться при повышенных температурах или в присутствии веществ, безусловно смертельных для других видов микроорганизмов.
Задача получения таких промышленных штаммов очень важна, для их видоизменения и отбора разработаны многочисленные приёмы активного воздействия на клетку - от обработки сильнодействующими ядами, до радиоактивного облучения. Цель этих приёмов одна - добиться изменения наследственного, генетического аппарата клетки. Их результат - получение многочисленных микробов-мутантов, из сотен и тысяч которых учёные потом стараются отобрать наиболее подходящие для той или иной цели. Создание приёмов химического или радиационного мутагенеза было выдающимся достижением биологии и широко применяется в современной биотехнологии .
Но их возможности ограничиваются природой самих микроорганизмов. Они не способны синтезировать ряд ценных веществ, которые накапливаются в растениях, прежде всего в лекарственных и эфирномасличных. Не могут синтезировать вещества, очень важные для жизнедеятельности животных и человека, ряд ферментов, пептидные гормоны, иммунные белки, интерфероны да и многие более просто устроенные соединения, которые синтезируются в организмах животных и человека. Разумеется, возможности микроорганизмов далеко не исчерпаны. Из всего изобилия микроорганизмов использована наукой, и особенно промышленностью, лишь ничтожная доля. Для целей селекции микроорганизмов большой интерес представляют, например, бактерии анаэробы , способные жить в отсутствие кислорода, фототрофы, использующие энергию света подобно растениям, хемоавтотрофы, термофильные бактерии, способные жить при температуре, как обнаружилось недавно, около 110 °C, и др.
И всё же ограниченность «природного материала» очевидна. Обойти ограничения пытались и пытаются с помощью культур клеток и тканей растений и животных. Это очень важный и перспективный путь, который также реализуется в биотехнологии . За последние несколько десятилетий учёные создали методы, благодаря которым отдельные клетки тканей растения или животного можно заставить расти и размножаться отдельно от организма, как клетки бактерий. Это было важное достижение - полученные культуры клеток используют для экспериментов и для промышленного получения некоторых веществ, которые с помощью бактериальных культур получить невозможно.
История развития и достигнутый уровень технологии
Во второй половине XX века было сделано несколько важных открытий и изобретений, лежащих в основе генной инженерии . Успешно завершились многолетние попытки «прочитать» ту биологическую информацию, которая «записана» в генах. Эта работа была начата английским учёным Ф. Сенгером и американским учёным У. Гилбертом (Нобелевская премия по химии г.). Как известно, в генах содержится информация-инструкция для синтеза в организме молекул РНК и белков, в том числе ферментов. Чтобы заставить клетку синтезировать новые, необычные для неё вещества, надо чтобы в ней синтезировались соответствующие наборы ферментов. А для этого необходимо или целенаправленно изменить находящиеся в ней гены, или ввести в неё новые, ранее отсутствовавшие гены. Изменения генов в живых клетках - это мутации. Они происходят под действием, например, мутагенов - химических ядов или излучений. Но такие изменения нельзя контролировать или направлять. Поэтому учёные сосредоточили усилия на попытках разработать методы введения в клетку новых, совершенно определённых генов, нужных человеку.
Основные этапы решения генноинженерной задачи следующие:
1. Получение изолированного гена. 2. Введение гена в вектор для переноса в организм. 3. Перенос вектора с геном в модифицируемый организм. 4. Преобразование клеток организма. 5. Отбор генетически модифицированных организмов (ГМО ) и устранение тех, которые не были успешно модифицированы.
Процесс синтеза генов в настоящее время разработан очень хорошо и даже в значительной степени автоматизирован. Существуют специальные аппараты, снабжённые ЭВМ, в памяти которых закладывают программы синтеза различных нуклеотидных последовательностей. Такой аппарат синтезирует отрезки ДНК длиной до 100-120 азотистых оснований (олигонуклеотиды). Получила распространение техника, позволяющая использовать для синтеза ДНК , в том числе мутантной, полимеразную цепную реакцию . Термостабильный фермент, ДНК-полимераза, используется в ней для матричного синтеза ДНК , в качестве затравки которого применяют искусственно синтезированные кусочки нуклеиновой кислоты - олигонуклеотиды. Фермент обратная транскриптаза позволяет с использованием таких затравок (праймеров) синтезировать ДНК на матрице выделенной из клеток РНК . Синтезированная таким способом ДНК называется комплементарной (РНК) или кДНК. Изолированный, «химически чистый» ген может быть также получен из фаговой библиотеки. Так называется препарат бактериофага , в геном которого встроены случайные фрагменты из генома или кДНК, воспроизводимые фагом вместе со всей своей ДНК .
Техника введения генов в бактерии была разработана после того, как Фредерик Гриффит открыл явление бактериальной трансформации . В основе этого явления лежит примитивный половой процесс, который у бактерий сопровождается обменом небольшими фрагментами нехромосомной ДНК , плазмидами . Плазмидные технологии легли в основу введения искусственных генов в бактериальные клетки.
Значительные трудности были связаны с введением готового гена в наследственный аппарат клеток растений и животных. Однако в природе наблюдаются случаи, когда чужеродная ДНК (вируса или бактериофага) включается в генетический аппарат клетки и с помощью её обменных механизмов начинает синтезировать «свой» белок. Учёные исследовали особенности внедрения чужеродной ДНК и использовали как принцип введения генетического материала в клетку. Такой процесс получил название трансфекция .
Если модификации подвергаются одноклеточные организмы или культуры клеток многоклеточных, то на этом этапе начинается клонирование , то есть отбор тех организмов и их потомков (клонов), которые подверглись модификации. Когда же поставлена задача получить многоклеточные организмы, то клетки с изменённым генотипом используют для вегетативного размножения растений или вводят в бластоцисты суррогатной матери, когда речь идёт о животных. В результате рождаются детеныши с изменённым или неизменным генотипом , среди которых отбирают и скрещивают между собой только те, которые проявляют ожидаемые изменения.
Применение в научных исследованиях
Хотя и в небольшом масштабе, генная инженерия уже используется для того, чтобы дать шанс забеременеть женщинам с некоторыми разновидностями бесплодия. Для этого используют яйцеклетки здоровой женщины. Ребёнок в результате наследует генотип от одного отца и двух матерей.
Однако возможность внесения более значительных изменений в геном человека сталкивается с рядом серьёзных этических проблем
11 Июля 2008Генная инженерия (генетическая инженерия) – совокупность методов и технологий, в том числе технологий получения рекомбинантных рибонуклеиновых и дезоксирибонуклеиновых кислот, по выделению генов из организма, осуществлению манипуляций с генами и введению их в другие организмы .
Генная инженерия – составная часть современной биотехнологии, теоретической основой ее является молекулярная биология, генетика. Суть новой технологии заключается в направленном, по заранее заданной программе конструировании молекулярных генетических систем вне организма (in vitro) с последующим внедрением созданных конструкций в живой организм. В результате достигается их включение и активность в данном организме и у его потомства. Возможности генной инженерии – генетическая трансформация, перенос чужеродных генов и других материальных носителей наследственности в клетки растений, животных и микроорганизмов, получение генно-инженерно-модифицированных (генетически модифицированных, трансгенных) организмов с новыми уникальными генетическими, биохимическими и физиологическими свойствами и признаками, делают это направление стратегическим.
С точки зрения методологии генная инженерия сочетает в себе фундаментальные принципы (генетика, клеточная теория, молекулярная биология, системная биология), достижения самых современных постгеномных наук: геномики, метаболомики, протеомики с реальными достижениями в прикладных направлениях: биомедицина, агробиотехнология, биоэнергетика, биофармакология, биоиндустрия и т.д.
Генная инженерия относится (наряду с биотехнологией, генетикой, молекулярной биологией, и рядом других наук о жизни) к сфере естественных наук.
Историческая справка
Генная инженерия появилась благодаря работам многих исследователей в разных отраслях биохимии и молекулярной генетики. В 1953 году Дж. Уотсон и Ф. Крик создали двуспиральную модель ДНК, на рубеже 50 – 60-х годов 20 века были выяснены свойства генетического кода, а к концу 60-х годов его универсальность была подтверждена экспериментально. Шло интенсивное развитие молекулярной генетики, объектами которой стали E.coli, ее вирусы и плазмиды. Были разработаны методы выделения высокоочищенных препаратов неповрежденных молекул ДНК, плазмид и вирусов. ДНК вирусов и плазмид вводили в клетки в биологически активной форме, обеспечивая ее репликацию и экспрессию соответствующих генов. В 1970 году Г.Смитом был впервые выделен ряд ферментов – рестриктаз, пригодных для генно-инженерных целей. Г.Смит установил, что полученный из бактерий очищенный фермент HindII сохраняет способность разрезать молекулы нуклеиновых кислот (нуклеазная активность), характерную для живых бактерий. Комбинирование ДНК-рестриктаз (для разрезания молекул ДНК на определенные фрагменты) и выделенных еще в 1967 г. ферментов – ДНК-лигаз (для «сшивания» фрагментов в произвольной последовательности) по праву можно считать центральным звеном в технологии генной инженерии.
Таким образом, к началу 70-х годов были сформулированы основные принципы функционирования нуклеиновых кислот и белков в живом организме и созданы теоретические предпосылки генной инженерии
Академик А.А. Баев был первым в нашей стране ученым, который поверил в перспективность генной инженерии и возглавил исследования в этой области. Генетическая инженерия (по его определению) – конструирование in vitro функционально активных генетических структур (рекомбинантных ДНК), или иначе – создание искусственных генетических программ.
Задачи и методы генной инженерии
Хорошо известно, что традиционная селекция имеет целый ряд ограничений, которые препятствуют получению новых пород животных, сортов растений или рас практически ценных микроорганизмов:
1. отсутствие рекомбинации у неродственных видов. Между видами существуют жесткие барьеры, затрудняющие естественную рекомбинацию.
2. невозможность управлять процессом рекомбинации в организме извне. Отсутствие гомологии между хромосомами приводит к неспособности сближаться и обмениваться отдельными участками (и генами) в процессе образования половых клеток. В результате становится невозможным перенос нужных генов и обеспечение оптимального сочетания в новом организме генов, полученных от разных родительских форм;
3. невозможность точно задать признаки и свойства потомства, т.к. процесс рекомбинации – статистический.
Природные механизмы, стоящие на страже чистоты и стабильности генома организма, практически невозможно преодолеть методами классической селекции.
Технология получения генетически модифицированных организмов (ГМО) принципиально решает вопросы преодоления всех естественных и межвидовых рекомбинационных и репродуктивных барьеров. В отличие от традиционной селекции, в ходе которой генотип подвергается изменениям лишь косвенно, генная инженерия позволяет непосредственно вмешиваться в генетический аппарат, применяя технику молекулярного клонирования. Генная инженерия позволяет оперировать любыми генами, даже синтезированными искусственно или принадлежащими не родственным организмам, переносить их от одного вида к другому, комбинировать в произвольном порядке.
Технология включает несколько этапов создания ГМО:
1. Получение изолированного гена.
2. Введение гена в вектор для встраивания в организм.
3. Перенос вектора с конструкцией в модифицируемый организм-рецепиент.
4. Молекулярное клонирование.
5. Отбор ГМО.
Первый этап – синтез, выделение и идентификация целевых фрагментов ДНК или РНК и регуляторных элементов очень хорошо разработан и автоматизирован. Изолированный ген может быть также получен из фаговой библиотеки.
Второй этап – создание in vitro (в пробирке) генетической конструкции (трансгена), которая содержит один или несколько фрагментов ДНК (кодирующих последовательность аминокислот белков) в совокупности с регуляторными элементами (последние обеспечивают активность трансгенов в организме). Далее трансгены встраивают в ДНК вектора для клонирования, используя инструментарий генной инженерии – рестриктазы и лигазы. За открытие рестриктаз Вернер Арбер, Даниел Натанс и Хамилтон Смит были удостоены Нобелевской премии (1978 г.). Как правило, в качестве вектора используют плазмиды – небольшие кольцевые молекулы ДНК бактериального происхождения.
Следующий этап – собственно «генетическая модификация» (трансформация), т.е. перенос конструкции «вектор – встроенная ДНК» в отдельные живые клетки. Введение готового гена в наследственный аппарат клеток растений и животных представляет собой сложную задачу, которая была решена после изучения особенностей внедрения чужеродной ДНК (вируса или бактерии) в генетический аппарат клетки. Процесс трансфекции был использован как принцип введения генетического материала в клетку.
Если трансформация прошла успешно, то после эффективной репликации из одной трансформированной клетки возникает множество дочерних клеток, содержащих искусственно созданную генетическую конструкцию. Основой для появления у организма нового признака служит биосинтез новых для организма белков – продуктов трансгена, например, растений – устойчивости к засухе или насекомым-вредителям у ГМ растений.
Для одноклеточных организмов процесс генетической модификации ограничивается встраиванием рекомбинантной плазмиды с последующим отбором модифицированных потомков (клонов). Для высших многоклеточных организмов, например, растений, то обязательным является включение конструкции в ДНК хромосом или клеточных органелл (хлоропластов, митохондрий) с последующей регенерацией целого растения из отдельной изолированной клетки на питательных средах. В случае животных, клетки с измененным генотипом вводят в бластоциды суррогатной матери. Первые ГМ растения были получены в 1982 году учеными из Института растениеводства в Кельне и компании Monsanto.
Основные направления
Постгеномная эра в первой декаде XXI-ого века подняла на новый уровень развитие генной инженерии. Так называемый Кельнский Протокол «На пути к биоэкономике, основанной на знаниях» , определил биоэкономику как «преобразование знаний наук о жизни в новую, устойчивую, экологически эффективную и конкурентоспособную продукцию». Дорожная карта генной инженерии содержит целый ряд направлений: генотерапия, биоиндустрия, технологии, основанные на стволовых клетках животных, ГМ растения, ГМ животные и т.д.
Генетически модифицированные растения
Ввести чужеродную ДНК в растения можно различными способами.
Для двудольных растений существует естественный вектор для горизонтального переноса генов: плазмиды агробактерий. Что касается однодольных, то, хотя в последние годы достигнуты определенные успехи в их трансформации агробактериальными векторами, все же подобный путь трансформации встречает существенные затруднения.
Для трансформации устойчивых к агробактериям растений разработаны приемы прямого физического переноса ДНК в клетку они включают: бомбардировку микрочастицами или баллистический метод; электропорацию; обработку полиэтиленгликолем; перенос ДНК в составе липосом и др.
После проведения тем или иным способом трансформации растительной ткани ее помещают in vitro на специальную среду с фитогормонами, способствующую размножению клеток. Среда обычно содержит селективный агент, в отношении которого трансгенные, но не контрольные клетки приобретают устойчивость. Регенерация чаще всего проходит через стадию каллуса, после чего при правильном подборе сред начинается органогенез (побегообразование). Сформированные побеги переносят на среду укоренения, часто также содержащую селективный агент для более строгого отбора трансгенных особей.
Первые трансгенные растения (растения табака со встроенными генами из микроорганизмов) были получены в 1983 г. Первые успешные полевые испытания трансгенных растений (устойчивые к вирусной инфекции растения табака) были проведены в США уже в 1986 г.
После прохождения всех необходимых тестов на токсичность, аллергенность, мутагенность и т.д. первые трансгенные продукты появились в продаже в США в 1994 г. Это были томаты Flavr Savr с замедленным созреванием, созданные фирмой «Calgen», а также гербицид-устойчивая соя компании «Monsanto». Уже через 1-2 года биотехнологические фирмы поставили на рынок целый ряд генетически измененных растений: томатов, кукурузы, картофеля, табака, сои, рапса, кабачков, редиса, хлопчатника.
В РФ возможность получения трансгенного картофеля методом бактериальной трансформации с использованием Agrobacterium tumefaciens была показана в 1990 г.
В настоящее время получением и испытанием генетически модифицированных растений занимаются сотни коммерческих фирм во всем мире с совокупным капиталом более 100 миллиардов долларов. Генно-инженерная биотехнология растений уже стала важной отраслью производства продовольствия и других полезных продуктов, привлекающей значительные людские ресурсы и финансовые потоки.
В России под руководством академика К.Г. Скрябина (Центр «Биоинженерия» РАН) получены и охарактеризованы ГМ сорта картофеля Елизавета плюс и Луговской плюс, устойчивые к колорадскому жуку. По результатам проверки Федеральной службой по надзору в сфере защиты прав потребителей и благополучия человека на основании экспертного заключения ГУ НИИ питания РАМН данные сорта прошли государственную регистрацию, внесены в государственный реестр и разрешены для ввоза, изготовления и оборота на территории РФ.
Данные ГМ сорта картофеля принципиально отличается от обычных наличием в его геноме встроенного гена, определяющего 100%-ю защиту урожая от колорадского жука без использования каких-либо химических средств.
Первая волна трансгенных растений, допущенных для практического применения, содержала дополнительные гены устойчивости (к болезням, гербицидам, вредителям, порче при хранении, стрессам).
Нынешний этап развития генетической инженерии растений получил название «метаболическая инженерия». При этом ставится задача не столько улучшить те или иные имеющиеся качества растения, как при традиционной селекции, сколько научить растение производить совершенно новые соединения, используемые в медицине, химическом производстве и других областях. Этими соединениями могут быть, например, особые жирные кислоты, полезные белки с высоким содержанием незаменимых аминокислот, модифицированные полисахариды, съедобные вакцины, антитела, интерфероны и другие «лекарственные» белки, новые полимеры, не засоряющие окружающую среду и многое, многое другое. Использование трансгенных растений позволяет наладить масштабное и дешевое производство таких веществ и тем самым сделать их более доступными для широкого потребления.
Генетически модифицированные животные
Клетки животных существенно отличаются от бактериальных по своей способности поглощать чужеродную ДНК, поэтому методы и способы способы введения генов в эмбриональные клетки млекопитающих, мух и рыб остаются в центре внимания генных инженеров.
Наиболее изученное в генетическом отношении млекопитающее – мыши. Первый успех относится к 1980 году, когда Д. Гордон с сотрудниками продемонстрировал возможность введения и интеграции чужеродной ДНК в геном мышей. Интеграция была стабильной и сохранялась у потомства. Трансформацию производят микроинъекцией клонированных генов в один или оба пронуклеуса (ядра) только что эмбриона на стадии одной клетки (зиготы). Чаще выбирают мужской пронуклеус, привнесенный сперматозоидом, так как его размеры больше. После инъекции яйцеклетку немедленно имплантируют в яйцевод приемной матери, или дают возможность развиваться в культуре до стадии бластоцисты, после чего имплантируют в матку.
Таким образом были инъецированы гены интерферона и инсулина человека, ген β-глобина кролика, ген тимидинкиназы вируса простого герпеса и кДНК вируса лейкемии мышей. Число молекул, вводимое за одну инъекцию, колеблется от 100 до 300 000, а их размер – от 5 до 50 кб. Выживает обычно 10 – 30% яйцеклеток, а доля мышей, родившихся из трансформированных яйцеклеток варьирует от нескольких до 40%. Таким образом, реальная эффективность составляет около 10%.
Таким методом получены генно-инженерные крысы, кролики, овцы, свиньи, козы, телята и другие млекопитающие. В нашей стране получены свиньи, несущие ген соматотропина. Они не отличались по темпам роста от нормальных животных, но изменение обмена веществ сказалось на содержании жира. У таких животных ингибировались процессы липогенеза и активировался синтез белка. К изменению обмена веществ приводило и встраивание генов инсулиноподобного фактора. ГМ свиньи были созданы для изучения цепочки биохимических превращений гормона, а побочным эффектом явилось укрепление иммунной системы.
Самая мощная белоксинтезирующая система находится в клетках молочной железы. Если поставить гены чужих белков под контроль казеинового промотора, то экспрессия этих генов будет мощной и стабильной, а белок будет накапливаться в молоке. С помощью животных-биореакторов (трансгенные коровы) уже получено молоко, в котором содержится человеческий белок лактоферрин. Этот белок планируется применять для профилактики гастроэнтерологических заболеваний у людей с низкой иммунорезистентностью: больные СПИДом, недоношенные младенцы, больные раком, прошедшие радиотерапию.
Важное направление трансгеноза – получение устойчивых к болезням животных. Ген интерферона, относящийся к защитным белкам, встраивали различным животным. Трансгенные мыши получили устойчивость – они не болели или болели мало, а вот у свиней такого эффекта не обнаружено.
Применение в научных исследованиях
Нокаут гена (gene knockout) – техника удаления одного или большего количества генов, что позволяет исследовать функции гена. Для получения нокаутных мышей полученную генно-инженерную конструкцию вводят в эмбриональные стволовые клетки, где конструкция подвергается соматической рекомбинации и замещает нормальный ген, а измененные клетки имплантируют в бластоцист суррогатной матери. Сходным способом получают нокаут у растений и микроорганизмов.
Искусственная экспрессия – добавление в организм гена, которого у него ранее не было, также с целями изучения функции генов. Визуализация продуктов генов – используется для изучения локализации продукта гена. Замещение нормального гена на сконструрованный ген, слитый с репортёрным элементом, (например, с геном зелёного флуоресцентного белка) обеспечивает визуализацию продукта генной модификации.
Исследование механизма экспрессии. Небольшой участок ДНК, расположенный перед кодирующей областью (промотор) и служащий для связывания факторов транскрипции, вводят в организм, поставив после него вместо собственного гена репортерный, например, GFP, катализирующий легко обнаруживаемую реакцию. Кроме того, что функционирование промотора в тех или иных тканях в тот или иной момент становится хорошо заметным, такие эксперименты позволяют исследовать структуру промотора, убирая или добавляя к нему фрагменты ДНК, а также искусственно усиливать экспрессию генов.
Биобезопасность генно-инженерной деятельности
Еще в 1975 г. ученые всего мира на Асиломарской конференции подняли важнейший вопрос: не окажет ли появление ГМО потенциально негативного воздействия на биологическое разнообразие? С этого момента одновременно с бурным развитием генной инженерии стало развиваться новое направление - биобезопасность. Главная ее задача - оценить не несет ли использование ГМО нежелательное воздействие на окружающую среду, здоровье человека и животных, а главная цель - открыть путь к использованию достижений современной биотехнологии, гарантируя при этом безопасность.
Стратегия биобезопасности основывается на научном исследовании особенностей ГМО, опыте обращения с ним, а также информации о его предполагаемом использовании и окружающей среде, в которую он будет интродуцирован. Совместными многолетними усилиями международных организаций (ЮНЕП, ВОЗ, ОЭСР), экспертов из разных стран, в т. ч. России, были разработаны базовые понятия и процедуры: биологическая безопасность, биологическая опасность, риск, оценка рисков. Только после того, как полный цикл проверок будет успешно осуществлен, готовится научное заключение о биобезопасности ГМО. В 2005 г. ВОЗ опубликовало доклад, согласно которому употребление зарегистрированных в качестве пищи ГМ растений также безопасно, как их традиционных аналогов.
Как обеспечивается биобезопасность в России? Началом включения России в мировую систему биобезопасности можно считать ратификацию «Конвенции о биоразнообразии» в 1995 году. С этого момента началось формирование национальной системы биобезопасности, отправной точкой которой явилось вступление в силу Федерального закона РФ «О государственном регулировании в области генно-инженерной деятельности» (1996 г.). ФЗ устанавливает основные понятия и принципы государственного регулирования и контроля всех видов работ с ГМО. ФЗ устанавливает уровни риска в зависимости от типа ГМО и вида работ, дает определения замкнутой и открытой систем, выпуска ГМО и т.д.
За прошедшие годы в России сформировалась одна из самых жестких систем регулирования. Неординарен тот факт, что система государственного регулирования ГМО стартовала превентивно, в 1996 году, до того, как реальные генно-инженерные организмы были заявлены для коммерциализации на территории России (первый ГМО – ГМ соя - была зарегистрирована для пищевого использования в 1999г.). Базовыми правовыми инструментами служат государственная регистрация генно-инженерно-модифицированных организмов, а также продукции, полученной из них или их содержащей, предназначенных для использования в качестве пищи и кормов.
Для понимания современной ситуации важен факт, что в течение 25 лет, прошедших с момента первого выхода ГМ растений на рынок, не было выявлено ни одного достоверного отрицательного воздействия их на окружающую среду и здоровье человека и животных ни в ходе испытаний, ни при коммерческом использовании. Только в одном из мировых источников – отчете авторитетного общества AGBIOS «Essential Biosafety» содержится более 1000 ссылок на исследования, доказывающие, что пища и корма, полученные из биотехнологических культур, настолько же безопасны, насколько безопасны и традиционные продукты. Однако на сегодняшний день в России отсутствует нормативно-правовая база, которая позволила бы осуществлять на территории нашей страны выпуск в окружающую среду ГМ растений, а также продукции, полученной из них или их содержащей. Как следствие – на 2010 год ни одно ГМ растение не выращивается на территории Российской Федерации в коммерческих целях.
По прогнозу, согласно Кельнскому Протоколу (2007 г), к 2030 г. отношение к сельскохозяйственным ГМ культурам изменится в сторону одобрения их использования.
Достижения и перспективы развития
Генная инженерия в медицине
Потребности здравоохранения, необходимость решения проблем старения населения формируют устойчивый спрос на генно-инженерные фармпрепараты (с годовым объемом продаж в 26 млрд. долл. США) и лечебно-косметические средства из растительного и животного сырья (с годовым объемом продаж около 40 млрд. долл. США).
Среди многих достижений генной инженерии, получивших применение в медицине, наиболее значительное – получение человеческого инсулина в промышленных масштабах.
В настоящее время по данным ВОЗ в мире насчитывается около 110 млн. людей, страдающих диабетом. Инсулин, инъекции которого показаны больным этим заболеванием, уже давно получают из органов животных и используют в медицинской практике. Однако многолетнее применение животного инсулина ведет к необратимому поражению многих органов пациента из-за иммунологических реакций, вызываемых инъекцией чужеродного человеческому организму животного инсулина. Но даже потребности в животном инсулине до недавнего времени удовлетворялись всего на 60 – 70%. Генные инженеры в качестве первой практической задачи клонировали ген инсулина. Клонированные гены человеческого инсулина были введены с плазмидой в бактериальную клетку, где начался синтез гормона, который природные микробные штаммы никогда не синтезировали. Начиная с 1982 года фирмы США, Японии, Великобритании и других стран производят генно-инженерный инсулин. В России получение генно-инженерного человеческого инсулина – Инсурана ведется в Институте биоорганической химии им. М.М. Шемякина и Ю.А. Овчинникова РАН. Сегодня отечественный инсулин производится в объеме, достаточном для обеспечения больных диабетом г. Москвы. Вместе с тем, потребность всего российского рынка в генно-инженерном инсулине удовлетворяется, в основном, импортными поставками. Мировой рынок инсулина составляет в настоящее время более 400 млн. долларов, ежегодное потребление около 2500 кг.
Развитие генной инженерии в 80-х годах прошлого столетия обеспечило хороший задел России в создании генно-инженерных штаммов микроорганизмов с заданными свойствами – продуцентов биологически активных веществ, в разработке генно-инженерных методов реконструирования генетического материала вирусов, в получении лекарственных субстанций, в том числе и с использованием компьютерного моделирования. До стадии производства доведены рекомбинантный интерферон и лекарственные формы на его основе медицинского и ветеринарного назначения, интерлейкин (b-лейкин), эритропоэтин. Несмотря на растущий спрос на высокоочищенные препараты, отечественное производство иммуноглобулинов, альбумина, плазмола обеспечивает 20% потребностей внутреннего рынка.
Активно ведутся исследования по разработке вакцин для профилактики и лечения гепатитов, СПИДа и ряда других заболеваний, а также конъюгированных вакцин нового поколения против наиболее социально значимых инфекций. Полимер-субъединичные вакцины нового поколения состоят из высокоочищенных протективных антигенов различной природы и носителя – иммуностимулятора полиоксидония, обеспечивающего повышенный уровень специфического иммунного ответа. Прививки против подавляющего большинства известных инфекций Россия могла бы обеспечить на базе собственного иммунологического производства. Полностью отсутствует только производство вакцины против краснухи.
Генная инженерия для сельского хозяйства
Генетическое улучшение сельскохозяйственных культур и декоративных растений представляет собой длительный и непрерывный процесс с использованием все более точных и предсказуемых технологий. В научном отчете ООН (за 1989 год) сказано следующее: «Поскольку молекулярные методы наиболее точны, те, кто их применяет, в большей степени уверены в том, какими признаками они наделяют растения, и, следовательно, реже получают незапланированные эффекты, чем при использовании обычных методов селекции.»
Преимущества новых технологий уже широко используются в таких странах, как США, Аргентина, Индия, Китай и Бразилия, где генетически модифицированные культуры возделывают на больших территориях.
Новые технологии также имеют большое значение для малоимущих фермеров и жителей бедных стран, особенно женщин и детей. Например, генетически модифицированные, устойчивые к вредителям, хлопчатник и кукуруза требуют применения инсектицидов в значительно меньших объемах (что делает труд на ферме более безопасным). Такие культуры способствуют повышению урожайности, получению фермерами более высоких доходов, снижению уровня бедности и риска отравления населения химическими пестицидами, что особенно характерно для ряда стран, в том числе для Индии, Китая, ЮАР и Филиппин.
Самыми распространенными ГМ растениями являются культуры, устойчивые к недорогим, наименее токсичным и наиболее широко используемым гербицидам. Возделывание таких культур позволяет получать более высокий урожай с гектара, избавиться от изнурительной ручной прополки, тратить меньше средств за счет минимальной или беспахотной обработки земли, что, в свою очередь, приводит к снижению эрозии почвы.
В 2009 году произошла замена генетически модифицированных культур первого поколения продуктами второго поколения, что впервые привело к увеличению урожайности per se. Пример биотехнологической культуры нового класса (над созданием которой работали многие исследователи) – устойчивая к глифосату соя RReady2Yield™ , выращивалась в 2009 году в США и Канаде более чем на 0.5 миллионах га.
Внедрение генной инженерии в современную агробиологию может быть проиллюстрировано следующими фактами из ряда зарубежных экспертных обзоров, в том числе, из ежегодного обзора независимой Международной службы по мониторингу за применением агробиотехнологий (ISAАA), возглавляемой известным в мире экспертом Клайвом Джеймсом (Claiv James): (www.isaaa.org)
В 2009 году в 25 странах мира выращивали ГМ культуры на площади 134 млн. га (что составляет 9% от 1,5 млрд. га всех пахотных земель в мире). Шесть стран ЕС (из 27) возделывали Bt кукурузу, и в 2009 году площади ее посевов достигли более 94 750 га. Анализ мирового экономического эффекта использования биотехнологических культур за период с 1996 по 2008 г.г. показывает рост прибыли в размере 51,9 миллиардов долларов благодаря двум источникам: во-первых, это сокращение производственных затрат (50%) и, во-вторых, значительная прибавка урожая (50%) в размере 167 миллионов тонн.
В 2009 году общая рыночная стоимость семян ГМ культур в мире составила 10.5 миллиардов долларов. Общая стоимость по зерну биотех кукурузы и сои, а также хлопчатника в 2008 году составила 130 млрд. долларов, и ожидается, что ее ежегодный рост составит 10 – 15%.
Подсчитано, что в случае полного принятия биотехнологии, к концу периода 2006 – 2015 г. прибыль всех стран в пересчете на ВВП вырастет на 210 млрд. долл. США в год.
Наблюдения, проводимые с начала применения в сельском хозяйстве устойчивых к гербицидам сельскохозяйственных культур, убедительно доказывают, что фермеры получили возможность более эффективно бороться с сорняками. При этом рыхление и распахивание полей утрачивают свое значение как средства борьбы с сорняками. В итоге снижается расход тракторного топлива, улучшается структура почвы и предотвращается ее эрозия. Целевые инсектицидные программы выращивания Bt хлопчатника предусматривают меньшее число опрыскиваний посевов и, следовательно, меньшее количество выездов техники на поля, что приводит к сокращению эрозии почв. Все это невольно содействует внедрению консервирующей технологии обработки почвы, направленной на снижение почвенной эрозии, уровня углекислого газа и уменьшения потери воды.
Для современного состояния науки характерен комплексный подход, создание единых технологических платформ для проведения широкого спектра исследований. Они объединяют не только биотехнологию, молекулярную биологию и генную инженерию, но также и химию, физику, биоинформатику, транскриптомику, протеомику, метаболомику.
Рекомендуемая литература
1. Дж. Уотсон. Молекулярная биология гена. М.: Мир. 1978.
2. Стент Г., Кэлиндар Р. Молекулярная генетика. М.: Мир. 1981
3. С.Н. Щелкунов «Генетическая инженерия». Новосибирск, издательство Сибирского Университета, 2008
4. Глик Б. Молекулярная биотехнология. Принципы и применение / Б. Глик, Дж. Пастернак. М.: Мир, 2002
5. Генная инженерия растений. Лабораторное руководство. Под редакцией Дж. Дрейпера, Р.Скотта, Ф. Армитиджа, Р. Уолдена. М.: «Мир». 1991.
6. Агробиотехнология в мире. Под ред. Скрябина К.Г. М.: Центр «Биоинженерия» РАН, 2008. – 135 с.
7. Кларк. Д., Рассел Л. Молекулярная биология простой и занимательный подход. М.: ЗАО «Компания КОНД». 2004
Ссылки
1. «О государственном регулировании генно-инженерной деятельности». ФЗ-86 в ред. 2000 г., ст.1
2. Кельнский Протокол, Cologne Paper, принят на конференции «На пути к Биоэкономике, основанной на знаниях» (Кельн, 30 мая 2007 г.), организованной Европейским Союзом в период президентства Германии в ЕС.

